
近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n。已知,最简单的氢铝化合物的分子式为Al2H6,它的熔点为150℃,燃烧热极高。Al2H6球棍模型如下图。下列有关说法肯定错误的是
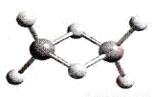
A.Al2H6在固态时所形成的晶体是分子晶体
B.氢铝化合物可能成为未来的储氢材料和火箭燃料
C.Al2H6中含有离子键和极性共价键
D.Al2H6在空气中完全燃烧,产物为氧化铝和水
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源:2015-2016学年内蒙古包头一中高二下学期期中考试化学试卷(解析版) 题型:选择题
分子式为C10H12O2的有机物,满足以下条件:①苯环上只有两个取代基;②与FeCl3溶液发生显色反应;③能发生银镜反应。则满足这些条件的有机物共有:
A.6种 B.9种 c.12种 D.15种
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省宜昌市高一下期中化学试卷(解析版) 题型:填空题
Ⅰ、 下列各组物质:①O2和O3 ②H2、D2、T2 ③12 C和14 C ④CH3CH2CH2CH3和(CH3)2CHCH3 ⑤癸烷和十六烷 ⑥CH3(CH2)5CH3和CH3CH2CH2CH(CH3)C2H5 (在横线上填相应的序号)
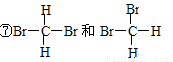
A、互为同位素的是_________ ; B、互为同分异构体的是________;
C、互为同素异形体的是________; D、同一种物质的是_________。
Ⅱ、 写出下列烷烃的分子式
(1)含有30个氢原子的烷 ;
(2)假如某烷烃的相对分子质量为142,则该烷烃的分子式为 ;
(3)烷烃A在同温同压下蒸气的密度是H2的36倍 ;
(4)1L烷烃D的蒸气完全燃烧时,生成同温同压下15L水蒸气 。
Ⅲ、甲烷的电子式为________,碳氢键之间键角为 。甲烷和氯气在光照下发生取代反应,生成___________种产物。产物中_________常用作灭火剂。试写出三溴甲烷在光照条件下与溴蒸气反应的化学方程式:____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省宜昌市高二下期中化学试卷(解析版) 题型:填空题
本题有三小题。
(1)已知N2,CO,H2O,NH3,CO2均为高中化学常见的分子,根据要求回答有关问题:
①根据等电子体原理,写出CO分子的结构式___________。
②试比较两分子中的键角大小:H2O___________NH3,(填“>”、“=”或“<” )
③基态N原子核外电子有 种不同的运动状态, B、C、N、O的第一电离能由大到小的顺序为 .
(2)科学家合成了Si60、N60, Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则28 g Si60分子中π键的数目为 。
(3)①立方氮化硼结构和硬度都与金刚石相似,但熔点比金刚石低,原因是__________ 。
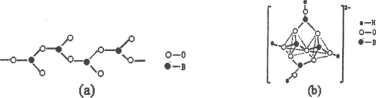
②在硼酸盐中,阴离子有链状、环状等多种结构形式。图(a)是一种链状结构的多硼酸根,则多硼酸根离子符号为________,图(b)是硼砂晶体中阴离子的环状结构,其中硼原子采取的杂化类型为_________。
(4) “嫦娥五号”探测器采用太阳能电池板提供能量,在太阳能电池板材料中除单晶硅外,还有铜,铟,镓,硒等化学物质,回答下列问题:
①SeO3分子的立体构型为 .
②金属铜投入氨水或H2O2溶液中均无明显现象,但投入氨水与H2O2的混合溶液中,则铜片溶解,溶液呈深蓝色,写出该反应的离子反应方程式为 .
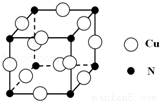
③某种铜合金的晶胞结构如图所示,该晶胞中距离最近的铜原子和氮原子间的距离为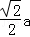 pm,则该晶体的密度为 (用含a的代数式表示,设NA为阿伏伽德罗常数的值).
pm,则该晶体的密度为 (用含a的代数式表示,设NA为阿伏伽德罗常数的值).
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省宜昌市高二下期中化学试卷(解析版) 题型:选择题
(Ⅲ)的八面体配合物CoClm·nNH3,若1 mol配合物与AgNO3作用生成1 mol AgCl沉淀,则m、n的值是( )
A.m=1,n=5 B.m=3,n=4 C.m=5,n=1 D.m=4,n=5
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省宜昌市高二下期中化学试卷(解析版) 题型:选择题
元素X、Y、Z原子序数之和为36,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构.下列推测不正确的是
A.同周期元素中X的金属性最强
B.原子半径X>Y,离子半径X+>Z2-
C.同族元素中Z的氢化物稳定性最高
D.同周期元素中Y的最高价含氧酸的酸性最强
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省襄阳市高一5月月考化学试卷(解析版) 题型:填空题
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:
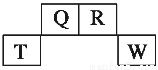
(1)T元素的离子结构示意图为__________。
(2)元素的非金属性(原子得电子的能力):Q ________W(填“强于”或“弱于”)。
(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,该反应的化学方程式为_________________________________________
(4)原子序数比R多1的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是_________________________________________________________其反应物的电子式为 。离子半径T3+__________R3-(填“>”、“<”、“=”)
(5)R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2 L的甲气体与0.5 L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐只有一种,则该含氧酸盐的化学式是____________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省襄阳市高一5月月考化学试卷(解析版) 题型:选择题
在一定条件下的密闭容器中,一定能说明可逆反应N2(g)+3H2(g) 2NH3(g)达到平衡状态的是( )
2NH3(g)达到平衡状态的是( )
A.混合气体的密度不再发生变化
B.反应速率之比υ(N2):υ(H2):υ(NH3)=1:3:2
C.每生成3molH2的同时消耗2molNH3
D.每断裂1molN≡N键的同时断裂6molN-H键
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省徐州市高二下第二次质量检测化学试卷(解析版) 题型:填空题
Q、R、X、Y、Z五种元素的原子序数依次递增。已知:①Z的原子序数为29,其余的均为短周期主族元素;②Y原子价电子(外围电子)排布msnmpn; ③R原子核外L层电子数为奇数;④Q、X原子p轨道的电子数分别为2和4。
请回答下列问题:(填写时用对应元素符号或物质的化学式)
(1)五种元素原子中基态时未成对电子数最多的是 。
(2)基态原子Y的轨道表示式是: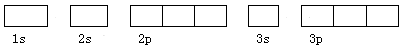
(3)基态原子Z 的电子排布式是 。向Z的硫酸盐溶液中加入过量氨水时反应的离子方程式是 ,所得产物中含Z元素在内的离子的结构示意图是:(不考虑空间构型,如有配位键,请标出)
(4)Q、R、X的电负性由小到大的顺序是 。
(5)Q、X和Y的氢化物稳定性由小到大的顺序为 。
(6)在一定条件下,原子的核外电子从激发态跃迁到基态产生的光谱属于 光谱(填“吸收”或“发射”),该光谱可用于 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com