
如下图所示,△H1=-393.5 kJ•mol-1,△H2=-395.4 kJ•mol-1,下列说法或表示式正确的是
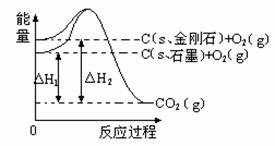
A. C(s、石墨)== C(s、金刚石) △H= +1.9 kJ•mol-1
B. 石墨和金刚石的转化是物理变化
C. 金刚石的稳定性强于石墨
D. 1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ
科目:高中化学 来源: 题型:
把6molA和5molB两气体通入容积为4L的密闭容器中,一定条件下反应:3A(g)+ B(g)  2C(g)+xD(g)DH<0 ;5min达平衡,此时生成2molC,测得D的平均反应速率为0.1mol·(L·min)-1.下列说法中正确的是
2C(g)+xD(g)DH<0 ;5min达平衡,此时生成2molC,测得D的平均反应速率为0.1mol·(L·min)-1.下列说法中正确的是
A. B的转化率为25%
B.A的平均反应速率为0.15mol·(L·min)-1
C.恒温下达到平衡的标志是C和D的生成速率相等
D.降低温度,逆反应速率变小,正反应速率增大,平衡正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
将SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个化学反应:
①SO2+2Fe3++2H2O=SO42-+2Fe2++4H+
②Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
下列有关说法错误的是
A.氧化性Cr2O72->Fe3+>SO2
B.K2Cr2O7能将Na2SO3氧化成Na2SO4
C.每有1molK2Cr2O7参加反应,转移电子的数目为6NA
D.若6.72 L SO2(标准状况)参加反应,则最终消耗0.2molK2Cr2O7
查看答案和解析>>
科目:高中化学 来源: 题型:
 化合物M是某种解热镇痛药,以A为原料的工业合成路线如下图所示:
化合物M是某种解热镇痛药,以A为原料的工业合成路线如下图所示:
|
 已知:
已知:

 ① +
① +  + CH3COOH
+ CH3COOH
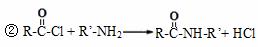
完成下列填空:
写出反应类型: 反应① 反应③ 。
A结构简式: 。由A合成D至少需要 个步骤才能完成。
写出反应④的化学方程式:
。
B的有苯环结构的同分异构体中有一种能在NaOH(aq)中发生水解。1mol该有机物最多消耗NaOH mol。写出满足下列条件所有的F的同分异构体的结构简式:
①是一种芳香族化合物; ②属α-氨基酸; ③苯环上有4种不同环境的氢原子
。 由 B不能一步完成,请解释可能的原因。
由 B不能一步完成,请解释可能的原因。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,两个恒容密闭容器中分别发生下列两个反应:①H2(g)+I2(g) 2HI(g) ②C(s)+H2O(g)
2HI(g) ②C(s)+H2O(g) CO(g)+H2(g),下列状态能表明两反应都达到平衡状态的是
CO(g)+H2(g),下列状态能表明两反应都达到平衡状态的是
a. 各物质的浓度不变 b. 容器内气体压强不变
c. 容器内气体密度不变 d. 容器内气体颜色不变
e. 各组分的物质的量分数或质量分数不变
A. abc B. ade C. ae D. ac
查看答案和解析>>
科目:高中化学 来源: 题型:
右图是某条件时N2与H2反应过程中能量变化的曲线图。下列叙述正确的是

A.该反应的热化学方程式为:2NH3  N2+3H2 ΔH =-92 kJ·mol-1
N2+3H2 ΔH =-92 kJ·mol-1
B.正反应的活化能大于逆反应的活化能
C.a曲线是未加入催化剂时的能量变化曲线
D.加入催化剂可增大正反应速率,降低逆反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
草酸与高锰酸钾在酸性条件下能够发生如下反应:
MnO4- + H2C2O4 + H+ —— Mn2+ + CO2↑+ H2O(未配平)
Ⅰ.甲同学研究外界因素对反应速率影响,设计如下实验方案:
用4 mL 0.001 mol/L KMnO4溶液与2 mL 0.01 mol/L H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
| 组别 | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
| A | 2 mL | 20 | |
| B | 2 mL | 20 | 10滴饱和MnSO4溶液 |
| C | 2 mL | 30 | |
| D | 1 mL | 20 | V1 mL蒸馏水 |
| E | 0.5 mL | 20 | V2 mL蒸馏水 |
(1)完成上述实验方案设计,其中: V1= ,V2= ;
(2) 如果研究温度对化学反应速率的影响,使用实验 和 。
(3) 甲同学在做A组实验时,发现反应开始时速率较慢,随后加快。他分析认为高锰酸钾与
草酸溶液的反应放热,导致溶液温度升高,反应速率加快;从影响化学反应速率的因素看,
你猜想还可能是 ;
Ⅱ.乙同学利用下图测定反应速率

回答下列问题
(4)实验时要检查装置的气密性,简述操作的方法是 ;
(5)乙同学通过生成相同体积的CO2来表示反应的速率,需要 仪来记录数据。
查看答案和解析>>
科目:高中化学 来源: 题型:
将SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个化学反应:
①SO2+2Fe3++2H2O=SO42-+2Fe2++4H+
②Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
下列有关说法错误的是
A.氧化性Cr2O72->Fe3+>SO2
B.K2Cr2O7能将Na2SO3氧化成Na2SO4
C.每有1molK2Cr2O7参加反应,转移电子的数目为6NA
D.若6.72 L SO2(标准状况)参加反应,则最终消耗0.2molK2Cr2O7
查看答案和解析>>
科目:高中化学 来源: 题型:
(Ⅰ)已知在448℃时,反应H2(g)+I2(g) 2HI(g)的平衡常数K1为49,则该温度下 反应
2HI(g)的平衡常数K1为49,则该温度下 反应 H2(g)+
H2(g)+ I2(g)
I2(g) HI(g)的平衡常数K2为__________。
HI(g)的平衡常数K2为__________。
(Ⅱ)在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=____________________。
(2)该反应为__________反应(填“吸热”或“放热”)。
(3)能判断该反应达到化学平衡状态的依据是( )。
A.容器中压强不变 B.混合气体中C(CO)不变
C.V(H2)正=V(H2O)逆 D. c(CO2)=c(CO)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com