
【题目】十九大报告提出“坚持保护环境,建设美丽中国”,下列物质不属于空气污染物的是
A. SO2 B. NO2 C. PM2.5 D. CO2
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:

(1)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体,写出④反应的离子方程式_____________;⑤反应的离子方程式______________;
(2)若A是应用最广泛的金属,④反应用到A,②⑤反应均用到同一种黄绿色气体单质。写出A与水反应的化学方程式__________________。④反应的离子方程式___________________;
D中加入氢氧化钠的现象是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[2017新课标Ⅰ]凯氏定氮法是测定蛋白质中氮含量的经典方法,其原理是用浓硫酸在催化剂存在下将样品中有机氮转化成铵盐,利用如图所示装置处理铵盐,然后通过滴定测量。已知:NH3+H3BO3=NH3·H3BO3;NH3·H3BO3+HCl= NH4Cl+ H3BO3。

回答下列问题:
(1)a的作用是_______________。
(2)b中放入少量碎瓷片的目的是____________。f的名称是__________________。
(3)清洗仪器:g中加蒸馏水;打开k1,关闭k2、k3,加热b,蒸气充满管路;停止加热,关闭k1,g中蒸馏水倒吸进入c,原因是____________;打开k2放掉水,重复操作2~3次。
(4)仪器清洗后,g中加入硼酸(H3BO3)和指示剂。铵盐试样由d注入e,随后注入氢氧化钠溶液,用蒸馏水冲洗d,关闭k3,d中保留少量水。打开k1,加热b,使水蒸气进入e。
①d中保留少量水的目的是___________________。
②e中主要反应的离子方程式为________________,e采用中空双层玻璃瓶的作用是________。
(5)取某甘氨酸(C2H5NO2)样品m 克进行测定,滴定g中吸收液时消耗浓度为c mol·L–1的盐酸V mL,则样品中氮的质量分数为_________%,样品的纯度≤_______%。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】北魏贾思勰《齐民要术·作酢法》这样描述:“乌梅去核,一升许肉,以五升苦酒渍数日,曝干,擣(同“捣”)作屑.欲食,辄投水中,即成醋尔.”下列有关醋的主要成分乙酸的说法中正确的是
A. 是一元酸 B. 0.lmol/L乙酸溶液的pH=l
C. 与乙醇反应时O-H键断裂 D. 含有双键,可使溴的四氯化碳溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【衡阳市2017届下学期第三次联考】碳、氮及其化合物是同学们经常能接触到的重要物质,是科学研究的重要对象。
(1)实验室制取乙炔的化学方程式为___________________________。
(2)H2NCOONH4是工业合成尿素的中间产物,该反应的能量变化如图A所示。用CO2和氨气合成尿素的热化学方程式为___________________________。
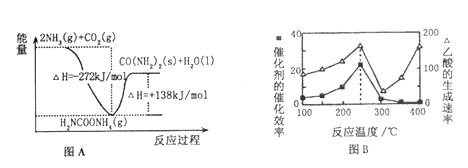
(3)合理利用CO2、CH4,抑制温室效应成为科学研究的新热点。一种以二氧化钛表面覆盖Cu2A12O4为催化剂,可以将CO2和CH4直接转化成乙酸(△H<0)。在不同温度下催化剂的催化效率与乙酸的生成速率分别如上图B所示。250~300℃时,温度升高而乙酸的生成速率降低的原因是________________。250℃和400℃时乙酸的生成速率几乎相等,实际生产中应选择的温度为_________℃。
(4)T℃时,将等物质的量的NO和CO充入体积为2L的 密闭容器中发生反应2NO+2CO![]() 2CO2+N2。保持温度和体积不变,反应过程中NO的物质的量随时间的变化如图C所示。
2CO2+N2。保持温度和体积不变,反应过程中NO的物质的量随时间的变化如图C所示。
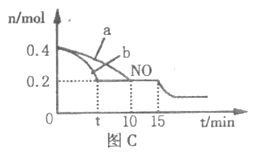
①平衡时若保持温度不变,再向容器中充入CO、N2各0.8mol,平衡将______(填“向左”、“向右”或“不”)移动。
②图中a、b分别表示在一定温度下,使用相同质量、不同表面积的催化剂时,达到平衡过程中n(NO)的变化曲线,其中表示催化剂表面积较大的曲线是______(填“a”或“b”)。
③15min时,若改变外界反应条件,导致n(NO)发生如图所示的变化,则改变的条件可能是_____________(任答一条即可)。
(5)垃圾渗滤液中含有大量的氨氮物质(用NH3表示)和氯化物,可用电解原理将溶液中的氨氮物质完全氧化除去。该过程分为两步:第一步:电解产生氯气;第二步:利用氯气将氨氮物质氧化为N2。
①第二步反应的化学方程式为____________________。
②若垃圾渗滤液中氨氮物质的质量分数为0.034% ,理论上用电解法净化It该污水,电路中转移的电子数为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于苯甲酸的重结晶实验,其结论或解释错误的是
选项 | 实验步骤 | 实验现象 | 结论或解释 |
A | 常温溶解 | 苯甲酸几乎不溶 | 苯甲酸常温时不溶于水或微溶于水 |
B | 加热溶解 | 苯甲酸完全溶解 | 温度升高,苯甲酸溶解度增大 |
C | 趁热过滤 | 过滤时伴有晶体析出 | 此晶体为杂质所形成 |
D | 冷却结晶,滤出晶体 | 针状晶体 | 针状晶体为苯甲酸 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于阿伏加德罗常数NA,下列说法正确的是( )
A. 浓硫酸催化,1mol乙醇与1.2mol醋酸充分反应可生产NA个乙酸乙酯分子
B. 0.1mol·L-1 HCOOH 电离得到NA个H+
C. 乙醛与足量的银氨溶液反应,一共断裂2NA个共价键
D. 铜催化下有1mol 2-丙醇全部转化为丙酮,失去2NA 个e-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com