
| 化学键 | P-P | P-O | P═O | O═O |
| 键能/kJ•mol-1 | a | b | c | d |
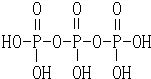 ,三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10.
,三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10.分析 (1)根据盖斯定律可知,将②×2-①即可得目标反应③;
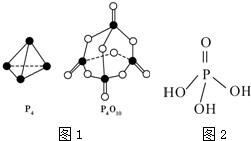
(2)白磷与氧气反应生成P4O10固体的化学方程式为:P4(s)+5O2(g)═P4O10(s),根据白磷和P4O10的空间结构可知,此反应断开6molP-P键、5molO=O键,形成4molP=O键和12molP-O键,据此分析;
(3)三聚磷酸可视为三个磷酸分子之间脱去两个水分子产物,则分子中含3个P,4个-OH;三聚磷酸中羟基的氢原子被钠离子取代生成三聚磷酸钠;
(4)设P4O10物质的量为x,P4O6物质的量为y,结合原子守恒计算得到.
解答 解:(1)已知反应反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)?(NH4)2CO3(aq)△H1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)?NH4HCO3(aq)△H2,根据盖斯定律可知,将II×2-I即可得目标反应III,故可得:反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)?2NH4HCO3(aq)△H3=2△H2-△H1,故答案为:2△H2-△H1;
(2)白磷与氧气反应生成P4O10固体的化学方程式为:P4(s)+5O2(g)═P4O10(s),根据白磷和P4O10的空间结构可知,此反应断开6molP-P键、5molO=O键,形成4molP=O键和12molP-O键,故有:P4(s)+5O2(g)═P4O10(s)
吸收:(6aKJ+5dKJ) 放出:(4c+12b)KJ
故有:△H=(6a+5d-4c-12b)KJ/mol=-( 4c+12b-6a-5d ) kJ•mol-1,故答案为:P4(s)+5O2(g)═P4O10(s)△H=-( 4c+12b-6a-5d ) kJ•mol-1;
(3)三聚磷酸可视为三个磷酸分子之间脱去两个水分子产物,其结构式为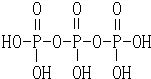 ;三聚磷酸中羟基的氢原子被钠离子取代生成三聚磷酸钠,三聚磷酸钠的化学式为:Na5P3O10,故答案为:
;三聚磷酸中羟基的氢原子被钠离子取代生成三聚磷酸钠,三聚磷酸钠的化学式为:Na5P3O10,故答案为: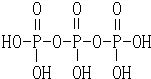 ;Na5P3O10;
;Na5P3O10;
(4)在某密闭容器中加入62g白磷和50.4L氧气(标准状况),白磷中磷原子物质的量=$\frac{62g}{31g/mol}$=2mol原子,氧气物质的量=$\frac{50.4L}{22.4L/mol}$=2.25mol,含有4.5mol氧原子;依据原子守恒列式计算:设P4O10物质的量为x,P4O6物质的量为y
4x+4y=2
5x+3y=2.25
计算出x=0.375mol,
y=0.125mol
最后生成0.375molP4O10,0.125molP4O6mol,故物质的量之比为3:1;
故答案为:3:1.
点评 本题考查了物质结构分析,热化学方程式书写和盖斯定律计算应用,原子守恒和化学方程式的计算方法应用,掌握基础是关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 0.15mol | B. | 0.0375mol | C. | 2.4g | D. | 19.2g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
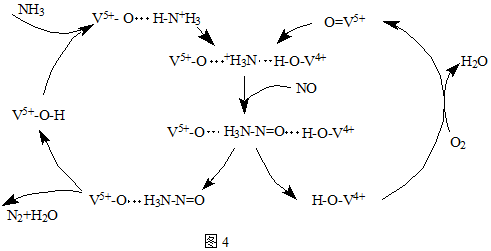
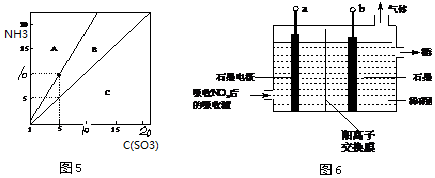
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 150 mL | B. | 200 mL | C. | 250 mL | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H=-2 878 kJ•mol-1 | B. | △H=-2 658 kJ•mol-1 | ||
| C. | △H=-1 746 kJ•mol-1 | D. | △H=-1 526 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤经处理变为气体燃料的过程属于物理变化 | |
| B. | 淀粉、油脂和蛋白质都是高分子化合物 | |
| C. | 乙烷和乙醇均能发生取代反应 | |
| D. | 乙酸乙酯和植物油均可水解生成乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
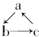 (“→”表示一步完成)关系相互转化的有( )
(“→”表示一步完成)关系相互转化的有( )| 物质 编号 | a | b | c |
| 1 | Al2O3 | NaAlO2 | Al(OH)3 |
| 2 | FeO | Fe(NO3)2 | Fe(OH)2 |
| 3 | MgCl2 | Mg(OH)2 | MgO |
| 4 | CuO | CuSO4 | Cu(OH)2 |
| 5 | Si | SiO2 | H2SiO3 |
| 6 | C | CO | CO2 |
| A. | 1项 | B. | 2项 | C. | 3项 | D. | 4项 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
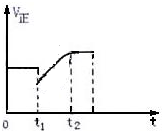 如图表示反应2SO2(g)+O2 $?_{加热}^{催化剂}$ 2SO3(g)+Q的正反应速率随时间的变化情况,试根据图曲线判断下列说法可能正确的是( )
如图表示反应2SO2(g)+O2 $?_{加热}^{催化剂}$ 2SO3(g)+Q的正反应速率随时间的变化情况,试根据图曲线判断下列说法可能正确的是( )| A. | t1时只减小了压强 | |
| B. | t1时只降低了温度 | |
| C. | t1时增加了SO2和O2的浓度,平衡向正反应方向移动 | |
| D. | t1时减小SO2浓度的同时,增加了SO3的浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑤ | B. | ②④⑤ | C. | ①②④ | D. | ②③⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com