
���� ij����M�����ȵ��ʸߡ������µ��Ե�Ժá������²���ǿ�ȴ������������ܣ�����⣬M��ֻ�������ֶ�����Ԫ�أ���ȡ41gM����������NaOH��Һ��ǡ�÷�Ӧ���õ���ɫ��ҺA��22.4L����B���������Ϊ��״���£�����������ʹ��ɫʯ����ֽ�������������B�ǰ���������Ӧ�����Һ����μ������ᣬ�ɹ۲쵽��Һ�ȱ���Ǻ����壬��Ӧ�����Һ������A��NaAlO2������Ԫ���غ�֪��M��AlN��
����B������ת����ϵ��B$\stackrel{x}{��}$C$\stackrel{x}{��}$D$\stackrel{H_{2}O}{��}$E��E��һ��ǿ�ᣬ��C��D�Ļ�����ܽ��ڽӽ���ȵ�ˮ�У����ɵõ�һ������F��ˮ��Һ��������������������һ��������һ��������������Ӧ���ɶ�������������������ˮ��Ӧ�������ᣬ����X��������C��NO��D�Ƕ���������E�����ᣬF�������ᣬ������ʵ��������������
��� �⣺ij����M�����ȵ��ʸߡ������µ��Ե�Ժá������²���ǿ�ȴ������������ܣ�����⣬M��ֻ�������ֶ�����Ԫ�أ���ȡ41gM����������NaOH��Һ��ǡ�÷�Ӧ���õ���ɫ��ҺA��22.4L����B���������Ϊ��״���£�����������ʹ��ɫʯ����ֽ�������������B�ǰ���������Ӧ�����Һ����μ������ᣬ�ɹ۲쵽��Һ�ȱ���Ǻ����壬��Ӧ�����Һ������A��NaAlO2������Ԫ���غ�֪��M��AlN��
����B������ת����ϵ��B$\stackrel{x}{��}$C$\stackrel{x}{��}$D$\stackrel{H_{2}O}{��}$E��E��һ��ǿ�ᣬ��C��D�Ļ�����ܽ��ڽӽ���ȵ�ˮ�У����ɵõ�һ������F��ˮ��Һ��������������������һ��������һ��������������Ӧ���ɶ�������������������ˮ��Ӧ�������ᣬ����X��������C��NO��D�Ƕ���������E�����ᣬF�������ᣬ
��1��ͨ�����Ϸ���֪��M��AlN���ʴ�Ϊ��AlN��
��2��A��NaAlO2��NaAlO2��ǿ�������Σ�ƫ���������ˮ�����Һ�ʼ��ԣ�ˮ�����ӷ���ʽΪAlO2-+2H2O?Al��OH��3+OH-��
�ʴ�Ϊ��AlO2-+2H2O?Al��OH��3+OH-��
��3������������Աȴ���ǿ���������������Ա�������ǿ��̼������������������ǿ����ȡ����֪��������̼����ȡ�����ᣬ���������ǿ�����ԣ���������л�ԭ�ԣ���������������ԭ��Ӧ����ѡbd��
��4������������Ӻ��������������ӷ�Ӧ����ƫ��������ӺͰ��������ӷ�Ӧ����ʽΪ2Al+NO2-+OH-+H2O=2AlO2-+NH3���������õ�ⷨ����ˮ��NO-2ת��ΪN2��ȥ����������õ������ɵ���������Ӧ�������������ɣ��缫��ӦʽΪ��2NO2-+6e-+4H2O=N2+8OH-��
�ʴ�Ϊ��2Al+NO2-+OH-+H2O=2AlO2-+NH3����������2NO2-+6e-+4H2O=N2+8OH-��
���� ���⿼�������ƶϣ�Ϊ��Ƶ���㣬���ؿ���ѧ�������ƶ��������漰�����ƶϡ�������ԭ��Ӧ�����ԭ��������ˮ���֪ʶ�㣬����������Ϊ���۽�����ʵ����ʽ����ƶϣ��������ջ���ԭ�����������ʣ���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��Ԫ�صĵ��ʼ��仯������о���Ӧ���ڹ�ũҵ���������ŷdz���Ҫ�ĵ�λ����ҵ���������Ҫ��Ӧ֮һ��
��Ԫ�صĵ��ʼ��仯������о���Ӧ���ڹ�ũҵ���������ŷdz���Ҫ�ĵ�λ����ҵ���������Ҫ��Ӧ֮һ��| Ũ��/mol��l-1 | C��NH3�� | C��O2�� | C��NO�� | C��H2O�� |
| ʱ��/min | ||||
| ��ʼ | 4.0 | 5.5 | 0 | 0 |
| ��2min | 3.2 | 4.5 | 0.8 | 1.2 |
| ��4min | 2.0 | 3.0 | 2.0 | 3.0 |
| ��6min | 3.0 | 3.0 | 2.0 | 3.0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
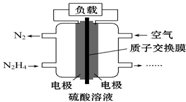 Һ��ȼ�ϵ�����������ȼ�ϵ�ؾ������С����������洢װ�õ��ŵ㣮һ�����£�N2H4��Ϊȼ�ϵĵ��װ����ͼ��ʾ���õ���ÿ����е�������Ϊ��������H2SO4��Ϊ����ʣ����й��ڸ�ȼ�ϵ�ص�������ȷ���ǣ�������
Һ��ȼ�ϵ�����������ȼ�ϵ�ؾ������С����������洢װ�õ��ŵ㣮һ�����£�N2H4��Ϊȼ�ϵĵ��װ����ͼ��ʾ���õ���ÿ����е�������Ϊ��������H2SO4��Ϊ����ʣ����й��ڸ�ȼ�ϵ�ص�������ȷ���ǣ�������| A�� | ���������缫�������غ������Ҳ�缫 | |
| B�� | ���������ĵ缫��ӦʽΪN2H4-4e-�TN2��+4H+ | |
| C�� | ���ø�ȼ�ϵ�ع�ҵ�Ͽ��Ե��MgCl2��Һ�Ʊ�Mg | |
| D�� | ��ȼ�ϵ�س����ŵ�ʱ���Ҳ���������缫��Ӧ����H+����c��H+����С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | KCl | B�� | CaCl2 | C�� | BaCl2 | D�� | AlCl3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  ��ͼ��ʾ��A��Ԫ�ص��⻯��ķе� | |
| B�� |  ��ͼ��ʾ��A��Ԫ�ص��۵� | |
| C�� |  ��ͼ��ʾNa+��Mg2+��Al3+�İ뾶 | |
| D�� |  ��ͼ��ʾ��������Ԫ�صĵ��ʵ��۵� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �ζ� ���� | ������Һ����� /mL | ����Һ�����/mL | |
| �ζ�ǰ�̶� | �ζ���̶� | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
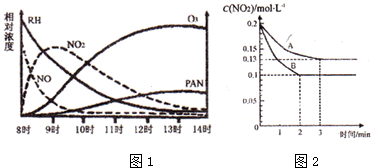
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com