
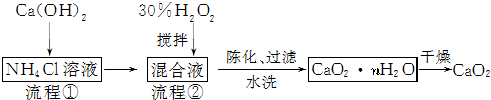

分析 由流程可知,在氯化铵溶液中加氢氧化钙,在搅拌条件下,加20%的H2O2溶液,CaCl2与氨气、过氧化氢发生反应生成CaO2•nH2O,CaO2•nH2O干燥得到CaO2,
(1)由化学反应中进行搅拌的目的以及防止物质分解或逸出来分析;CaCl2与氨气、过氧化氢发生反应生成CaO2•nH2O;
(2)工艺流程分析来判断循环使用的物质;
(3)溶液中含有氯离子,若洗液中没有氯离子说明洗涤干净,所以要检验洗液中是否含有氯离子;
(4)从图中看出:过氧化钙的质量是1.08g,则结晶水的质量=3.24g-1.08g=2.16g;根据式量比等于质量比计算.
解答 解:由流程可知,在氯化铵溶液中加氢氧化钙,在搅拌条件下,加20%的H2O2溶液,CaCl2与氨气、过氧化氢发生反应生成CaO2•nH2O,CaO2•nH2O干燥得到CaO2,
(1)在化学反应中进行搅拌能够加快反应速率;H2O2易分解,而且氨气易挥发,所以没有采用加热措施;CaCl2与氨气、过氧化氢发生反应生成CaO2•nH2O,其反应的方程式为:CaCl2+H2O2+2NH3+nH2O═CaO2•nH2O↓+2NH4Cl;
故答案为:加快反应速率;减少H2O2分解、防止氨气大量逸出;CaCl2+H2O2+2NH3+nH2O═CaO2•nH2O↓+2NH4Cl;
(2)工艺流程分析可知,开始用到氯化铵,制备CaO2•nH2O时又生成氯化铵,所以循环使用的物质是NH4Cl;
故答案为:NH4Cl;
(3)溶液中含有氯离子,若洗液中没有氯离子说明洗涤干净,所以要检验洗液中是否含有氯离子,其检验方法为取最后一次洗涤液少许于试管中,滴加HNO3酸化的AgNO3溶液,若无白色沉淀产生,说明洗涤干净;
故答案为:取最后一次洗涤液少许于试管中,滴加HNO3酸化的AgNO3溶液,若无白色沉淀产生,说明洗涤干净;
(4)从图中看出:过氧化钙的质量是1.08g,则结晶水的质量=3.24g-1.08g=2.16g;由化学式CaO2•nH2O可知,其中CaO2和结晶水的质量比为:
72:18n=1.08g:2.16g,解得n=8,所以化学式为:CaO2•8H2O;
答:过氧化钙晶体(CaO2•nH2O)的化学式为CaO2•8H2O.
点评 本题考查物质制备实验,涉及物质的性质、物质的检验及化学计算等问题,题目难度较大,做题时注意分析题中关键信息、明确实验流程中的反应、物质的量关系等为解答的关键,充分考查了学生的分析、化学实验、化学计算能力.


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸镁 | B. | 硫酸钡 | C. | 氢氧化镁 | D. | 碳酸钡 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据置换反应Na+KCl$\frac{\underline{\;高温\;}}{\;}$NaCl+K↑,推出金属Na的活泼性强于金属K的活泼性 | |
| B. | 根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7 | |
| C. | 根据金属活动顺序表推知Sn活泼性强于Pb,推出碱性Sn(OH)4>Pb(OH)4 | |
| D. | 根据较强酸可以制取较弱酸的规律,推出CO2通入NaClO溶液中能生成HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
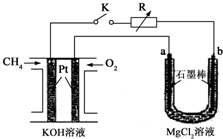 新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液.某研究小组将甲烷燃料电池作为电源进行氯化镁溶液电解实验,电解装置如图所示.请回答下列问题:
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液.某研究小组将甲烷燃料电池作为电源进行氯化镁溶液电解实验,电解装置如图所示.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 每一个水分子内含有两个氢键 | |
| B. | 水分子的空间构型为V形 | |
| C. | H2O是一种非常稳定的化合物,这是由于氢键所致 | |
| D. | 水是良好的溶剂,易溶解HCl、CH4等气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

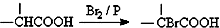
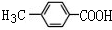 .
.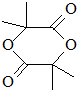 .
.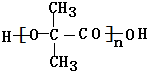 +(n-1)H2O,该反应属于缩聚反应(填反应类型).
+(n-1)H2O,该反应属于缩聚反应(填反应类型).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com