
【题目】同学们课外探究酸的性质活动中将以下8个实验分为三组进行(如下图所示)。
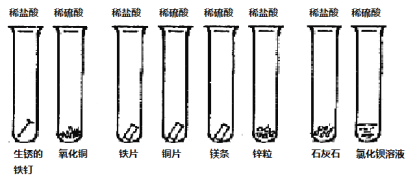
① ② ③ ④ ⑤ ⑥ ⑦ ⑧
(1)这8个实验是如何分组的?请写出各组的试管编号:第一组 第二组 第三组 ,你认为如此分组的依据是: 。
(2)写出试管②⑤的实验现象及有关的离子方程式:
② ; 。
⑤ ; 。
(3)请作为课外活动小组成员,根据实验及现象的分析、比较,归纳出的结论(至少答3条):
①___________________________________;
②___________________________________;
③____________________________________。
【答案】(1)第一组①②;第二组③④⑤⑥ ;第三组⑦⑧ ; 因为本实验的目的是研究强酸(盐酸和硫酸)分别与金属氧化物、金属、盐的反应,所以如此分类
(2)②固体溶解,得到蓝色的溶液;CuO+2H+=Cu2++H2O。
⑤镁条溶解,产生大量气体;Mg+2H+=Mg2++H2↑
(3)(共3分写出其中三个点给满分)①酸能跟某些金属氧化物反应;②酸能跟某些盐反应;③酸能跟多种活泼金属反应;④酸并不能跟所有金属反应;⑤酸与活泼金属反应时速度不同
【解析】
试题分析:(1)本实验的目的是探究酸的性质,①中生锈的铁钉主要成分是氧化铁,是氧化物,②中氧化铜是氧化物,③中铁片是金属,④中铜片是金属,⑤中镁条是金属,⑥中锌粒是金属,⑦中石灰石是盐,⑧中氯化钡是盐,根据与酸反应的类别,分为氧化物、金属、盐;
(2)②氧化铜与稀硫酸反应,生成硫酸铜和水,所以氧化铜固体溶解,生成的硫酸铜中铜离子的颜色为蓝色,反应的离子方程式为CuO+2H+=Cu2++H2O;
⑤镁条为金属单质,它和稀硫酸反应生成硫酸镁和氢气,所以镁条溶解,有气体生成,反应的离子方程式为Mg +2H+=Mg2++H2↑;
(3)在复分解反应中,若生成物中有水或气体或沉淀生成时,将会使生成物中的离子浓度减小,反应持续进行,探究酸的性质,须考虑酸能否与与之发生复分解反应,所以考虑酸与金属、氧化物、与某些盐反应。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下表是某食品包装上的说明,表中列出了部分配料。
品 名 | 乐百氏 |
部分配料 | ① 奶粉 ②白砂糖③ 乳酸钙 ④ 山梨酸钾 |
生产日期 | 标于包装封口处 |
配料中,富含蛋白质的是____(填序号,下同),属于营养强化剂的是___,属于防腐剂的是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH3CH2Br与NH3反应生成(CH3CH2)2NH和HBr,下列说法错误的是
A. 若原料完全反应成上述产物,n(CH3CH2Br) :n(NH3)=2:1 B. 该反应属于取代反应
C. CH3CH2Br难溶于水 D. CH3CH2Br和HBr均属于电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
A. 氨基酸脱水缩合产生水,水中的氢都来自氨基
B. 纤维素与脂肪都是由C、H、O三种元素组成的
C. 蛋白质是组成生物膜的主要成分,可被苏丹Ⅲ染液染成紫色
D. 组成RNA和DNA的元素种类不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一体积固定为10L的密闭恒温容器中充入1.5mol氨气,发生反应:2NH3(g)![]() N2(g)+3H2(g) △H=93KJ/mol
N2(g)+3H2(g) △H=93KJ/mol
反应容器中NH3物质的量随时间的变化如下图所示:

(1)2min时反应进入化学平衡状态,此时容器内物质浓度c(H2)=______mol/L。
(2)0~2min内以NH3表示的平均反应速率v(NH3)=________mol/(L·min)。
(3)依图中曲线判断、0~2min内NH3分解反应是_____(填“先快后慢”或“先慢后快”或“匀速进行”)。
(4)容器内起始时与平衡时的压强比为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸、硫酸和硝酸是中学阶段常见的“三大酸”。现就三大酸与金属铜反应的情况,回答下列问题:
(1)稀盐酸不与Cu 反应,若在稀盐酸中加入H2O2后,则可使铜顺利溶解。该反应的化学方程式为:___________________。
(2)在一定体积的10mol/L的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9mol。则浓硫酸的实际体积__________(填“大于”、“ 等于”或“小于”)180mL。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为________________。
(3)镁铁混合物4.9g,溶解在过量的某浓度的稀硝酸中,完全反应后得到标准状况下2 .24LNO气体。若向反应后的溶液中加入足量的烧碱,则可生成沉淀的质量是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纯锌跟稀H2SO4 反应速率很小,为了加快锌的溶解和放出H2 的速率,并且使产生H2 的量不变,当稀H2SO4 过量时,可向其中加少量
A、CuSO4 溶液 B、铜粉 C、ZnSO4 D、镁条
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学研究发现,苹果含有微量元素Zn,而锌是构成与记忆力息息相关的核酸和蛋白质不可缺少的元素。儿童缺锌就会导致大脑发育不良,因此苹果又被称为记忆之果。这说明无机盐离子
A. 对维持酸碱平衡有重要作用
B. 对维持细胞形态有重要作用
C. 对调节细胞内的渗透压有重要作用
D. 对维持生物体的生命活动有重要作用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com