
【题目】元素周期表是学习化学的重要工具,它隐含着许多信息和规律.根据下表中短周期元素的原子半径和主要化合价,回答表后的问题.
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
原子半径(10﹣10m) | 0.74 | 1.60 | 0.53 | 1.10 | 0.99 | 1.11 | 0.75 | 1.43 |
最高或最低化合价 | +2 | +1 | +5 | +7 | +2 | +5 | +3 | |
﹣2 | ﹣3 | ﹣1 | ﹣3 |
(1)上述元素中与元素⑧处于同一周期的有(填元素符号)
(2)元素①在元素周期表中的位置是
(3)①④⑦三种元素的氢化物的稳定性由强到弱的顺序为(填化学式)
(4)请写出下列元素形成的常见化合物的电子式: ③⑤②⑤③⑦
(5)请写出⑤⑧两种元素的最高价氧化物对应水化物间反应的离子方程式: .
【答案】
(1)Mg、P、Cl
(2)第二周期ⅥA族
(3)H2O>NH3>PH3
(4)![]() ;
;![]() ;
;
(5)3H++Al(OH)3═Al3++3H2O
【解析】解:(1)上述元素中与元素⑧是铝,处于同三周期的有 Mg、P、Cl,所以答案是:Mg、P、Cl;(2)元素①是氧在元素周期表中的位置是第二周期第ⅥA族,所以答案是:第二周期第ⅥA族;(3)非金属性越强,氢化物越稳定,①④⑦三种元素的氢化物的稳定性由强到弱的顺序为H2O>NH3>PH3 , 所以答案是:H2O>NH3>PH3;(4)请写出下列元素形成的常见化合物的电子式:③⑤形成的常见化合物是HCl,氯化氢为共价化合物,其电子式为为 ![]() ;②⑤形成的常见化合物是MgCl2 , 氯化镁为离子化合物,其电子式为
;②⑤形成的常见化合物是MgCl2 , 氯化镁为离子化合物,其电子式为 ![]() ;③⑦形成的常见化合物NH3 , 氨气为共价化合物,其电子式为
;③⑦形成的常见化合物NH3 , 氨气为共价化合物,其电子式为  ,所以答案是:
,所以答案是: ![]() ;
; ![]() ;
;  ;(5)请写出⑤⑧两种元素的最高价氧化物对应水化物分别是高氯酸和氢氧化铝,它们之间反应的离子方程式:3H++Al(OH)3═Al3++3H2O, 所以答案是:3H++Al(OH)3═Al3++3H2O.
;(5)请写出⑤⑧两种元素的最高价氧化物对应水化物分别是高氯酸和氢氧化铝,它们之间反应的离子方程式:3H++Al(OH)3═Al3++3H2O, 所以答案是:3H++Al(OH)3═Al3++3H2O.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】将铜和镁组成的2.24g混合物投入适量某浓度的硝酸中完全反应,还原产物中有NO2、NO、N2O三种气体,且体积均为0.224L(标准状况),然后向反应后的溶液中,加入足量的NaOH溶液,所得沉淀经过滤、洗涤、干燥后称量,质量为
A. 3.12g B. 4.28g C. 4.68g D. 5.08g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中充入CO2、CO、CH4的混合气体共m g,若加入足量Na2O2,充分振荡并不断用电火花引燃至反应完全,测得固体质量增加m g,则CO2与CH4的体积比为( )
A.3∶1B.2∶1C.1∶1D.任意比
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I 已知:HCN(aq)+NaOH(aq)═NaCN(aq)+H2O(l)△H=﹣12.1kJmol﹣1;HCl(aq)+NaOH(aq)═NaCl(aq)+H2O(l)△H=﹣55.6kJmol﹣1。则在水溶液中HCN![]() H++ CN-电离的△H为_______________kJmol﹣1
H++ CN-电离的△H为_______________kJmol﹣1
II 用右图所示装置进行中和热测定实验,请回答下列问题:
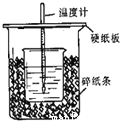
(1)大小烧杯之间填满碎泡沫塑料的作用是_____________,从实验装置上看,图中缺少的一种玻璃仪器______________。
(2)实验中若用60mL0.25mol·L-1H2SO4溶液跟50mL0.55mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量___________ (填“相等”.“不相等”),所求中和热______________ (填“相等”.“不相等”),若用50mL0.50mol·L-1醋酸代替H2SO4溶液进行上述实验,测得反应前后温度的变化值会_____________ (填“偏大”、“偏小”、“不受影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,合成氨工业在国民生产中有重要意义。以下是关于合成氨的有关问题,请回答:
(1)若在一容积为2 L的密闭容器中加入0.2 mol的N2和0.6 mol的H2,在一定条件下发生反应: N2(g) +3H2(g)![]() 2NH3(g) ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2 mol。则前5分钟的平均反应速率v(N2)=________。
2NH3(g) ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2 mol。则前5分钟的平均反应速率v(N2)=________。
(2)平衡后,若要提高H2的转化率,可以采取的措施有________。
A.加了催化剂 B.增大容器体积 C.降低反应体系的温度 D.加入一定量N2
(3)若在0.5 L的密闭容器中,一定量的氮气和氢气进行如下反应:N2(g)+3H2(g)![]() 2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示:
2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示:
T/℃ | 200 | 300 | 400 |
K | K1 | K3 | 0.5 |
请完成下列问题:
①试比较K1、K2的大小,K1________K2(填“<”、“>”或“=”);
②下列各项能作为判断该反应达到化学平衡状态的依据是________(填序号字母)
A.容器内N2、H2、NH3的物质的量浓度之比为1∶3∶2
B.v(H2)正=3v(H2)逆
C.容器内压强保持不变
D.混合气体的密度保持不变
③400℃时,反应2NH3(g)![]() N2(g)+3H2(g)的化学平衡常数为________。当测得NH3、N2和H2物质的量分别为3 mol、2 mol和 1 mol时,则该反应的v(N2)正________v(N2)逆(填“<”、“>”或“=”)。
N2(g)+3H2(g)的化学平衡常数为________。当测得NH3、N2和H2物质的量分别为3 mol、2 mol和 1 mol时,则该反应的v(N2)正________v(N2)逆(填“<”、“>”或“=”)。
(4)根据化学反应速率和化学平衡理论,联系合成氨的生产实际,你认为下列说法不正确的是________。
A.化学反应速率理论可指导怎样在一定时间内快出产品
B.勒夏特列原理可指导怎样使用有限原料多出产品
C.催化剂的使用是提高产品产率的有效方法
D.正确利用化学反应速率和化学反应限度理论都可以提高化工生产的综合经济效益
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】提纯下列物质所选试剂及对应分离方法均可行的是
物质 | 杂质 | 试剂 | 方法 | |
A | 乙烷 | 乙烯 | 酸性高锰酸钾溶液 | 洗气 |
B | 乙酸乙酯 | 乙酸 | 氢氧化钠溶液 | 洗涤分液 |
C | 溴苯 | 溴 | 碘化钾溶液 | 萃取分液 |
D | 乙醇 | 水 | 生石灰 | 蒸馏 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】任一定温度下的定容容器中,当下列物理量不再发生变化时,能说明I2(g)+H2(g) ![]() 2HI(g)能说明达到平衡状态的有几个:①混合气体的压强②混合气体的密度③混合气体的总物质的量④混合气体的平均相对分子质量⑤混合气体的颜色⑥各反应物或生成物的浓度之比等于化学计量数之比⑦某种气体的百分含量。
2HI(g)能说明达到平衡状态的有几个:①混合气体的压强②混合气体的密度③混合气体的总物质的量④混合气体的平均相对分子质量⑤混合气体的颜色⑥各反应物或生成物的浓度之比等于化学计量数之比⑦某种气体的百分含量。
A. 2个 B. 3个 C. 4个 D. 5个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物品或设备:①水泥路;②门窗玻璃;③水晶镜片;④石英钟表;⑤玛瑙手镯;⑥硅太阳能电池;⑦光导纤维;⑧计算机芯片。所用材料含有SiO2的是( )。
A.①②③④⑤⑦
B.①②⑦⑧
C.⑥⑧
D.全部
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com