
分析 发生Cu+4HNO3═Cu(NO3)2+2NO2↑+2H2O,n(NO2)=$\frac{4.48L}{22.4L/mol}$=0.2mol,由反应可知,生成二氧化氮对应的硝酸作氧化剂被还原,结合反应及c=$\frac{n}{V}$计算.
解答 解:(1)n(NO2)=$\frac{4.48L}{22.4L/mol}$=0.2mol,由电子守恒可知,n(Cu)=$\frac{0.2mol×(5-4)}{(2-0)}$=0.1mol,其质量为0.1mol×64g/mol=6.4g,
答:参加反应的铜的质量为6.4g;
(2)由反应可知,生成二氧化氮对应的硝酸作氧化剂被还原,由N原子守恒可知,被还原的硝酸的物质的量为0.2mol,
答:被还原的硝酸的物质的量为0.2mol;
(3)由Cu原子守恒可知,n[Cu(NO3)2]=0.1mol,则溶液中Cu(NO3)2的物质的量浓度为$\frac{0.1mol}{0.5L}$=0.2mol/L,
答:溶液中Cu(NO3)2的物质的量浓度为0.2mol/L.
点评 本题考查氧化还原反应的计算,为高频考点,把握发生的反应、电子及原子守恒为解答的关键,侧重分析与计算能力的考查,注意守恒法的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
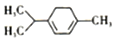
| A. | 该物质属于芳香族化合物,难溶于水 | |
| B. | 该物质可以发生消去、氧化、取代等反应 | |
| C. | 该分子结构中所有碳原子可能共平面 | |
| D. | 该有机物的一氯取代物有7种(不含立体结构) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 制备气体 | X(除杂试剂) | Y (检验试剂) | 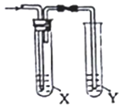 | |
| A | CH3CH2Br与NaOH乙醇溶液共热 | H2O | KMnO4酸性溶液 | |
| B | 电石与NaCl水溶液 | H2O | Br2的CCl4溶液 | |
| C | C2H5OH与浓硫酸 加热至170℃ | 饱和NaHSO3 溶液 | K2Cr2O7酸性溶液 | |
| D | 生石灰与浓氨水 | 浓硫酸 | 红色石蕊试纸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 反应时间(min) | 1 | 2 | 3 | 4 | 5 |
| 生成氢气体积(ml) | 50 | 150 | 300 | 380 | 410 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
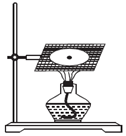 某化学实验小组拟用如图装置进行钠与氧气反应的实验.
某化学实验小组拟用如图装置进行钠与氧气反应的实验.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
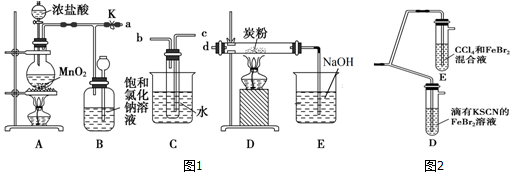
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 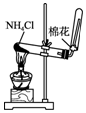 制备氨气 | B. | 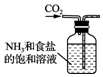 制取NaHCO3 | C. | 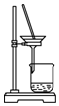 分离NaHCO3 | D. | 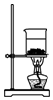 灼烧NaHCO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com