
| A. | 22.1 g | B. | 27.2 g | C. | 30 g | D. | 19.4 g |
分析 根据电子守恒计算出金属失去电子的物质的量,根据反应中金属失去电子的物质的量等于生成碱的氢氧根离子的物质的量,从金属单质转化为其氢氧化物,增加的是氢氧根离子的质量来计算生成沉淀的质量,但是不包括氢氧化铝.
解答 解:将合金溶于过量稀硝酸中,分别生成Al3+、Fe3+、Mg2+离子,根据电子守恒,金属共失去电子的物质的量和氮原子得电子的量是相等的,生成了6.72L NO,即氮原子得电子的物质的量是:$\frac{6.72L}{22.4L/mol}$×(5-2)=0.9mol,根据前后发生的整个过程的反应,知道反应中金属失去电子的物质的量等于生成碱的氢氧根离子的物质的量,即n(OH-)=0.9mol,从金属单质转化为其氢氧化物,增加的是氢氧根离子的质量,所以反应后沉淀的质量(包括氢氧化铝)等于11.9g+0.9mol×17g/mol=27.2g,但是加入过量氢氧化钠后,不会生成氢氧化铝沉淀,开始合金质量减少了2.7g,所以沉淀氢氧化铝的量是7.8g,最终所得沉淀的质量=27.2g-7.8g=19.4g,
故选D.
点评 本题考查混合物的计算,题目难度不大,注意从守恒的角度做题较为简单,试题培养了学生的分析能力及化学计算能力.


 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  图表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液 | |
| B. |  图表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化 | |
| C. |  图表示0.1000mol•L-1NaOH溶液滴定20.00mL0.1000mol•L-1醋酸溶液得到的滴定曲线 | |
| D. |  图是亚硫酸氢钠粉末投入稀硝酸溶液中有关图象 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
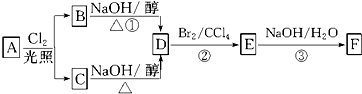
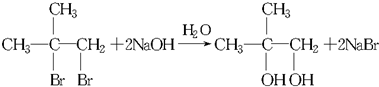 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
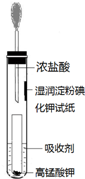 氯气是氯碱工业的主要产品之一,是一种常用的消毒剂,其消毒原理是与水反应生成了次氯酸:Cl2+H2O?HCl+HClO K=4.5×10-4
氯气是氯碱工业的主要产品之一,是一种常用的消毒剂,其消毒原理是与水反应生成了次氯酸:Cl2+H2O?HCl+HClO K=4.5×10-4查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 元素 | A | B | C |
| 性质或结构信息 | 工业上通过分离液态空气获得其单质,单质能助燃 | 气态氢化物的水溶液显碱性 | 原子有三个电子层,简单离子在本周期中半径最小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
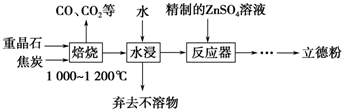
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com