
| A. | 锌为电池负极,发生氧化反应 | |
| B. | 电池工作时,氧气与锌直接化合,生成氧化锌 | |
| C. | 正极发生的反应是:$\frac{1}{2}$O2+2e-+2H+═H2O | |
| D. | 负极发生的反应是:Zn-2e-+H2O═ZnO+2H+ |
分析 根据总反应Zn+$\frac{1}{2}$O2═ZnO中化合价变化可知Zn被氧化,作原电池的负极,负极上锌失电子发生氧化反应,正极上氧气得电子发生还原反应,若电解质为酸性,正极电极反应为:$\frac{1}{2}$O2+2e-+2H+═H2O,总反应减去正极得到负极反应:Zn-2e-+H2O═ZnO+2H+,以此解答该题.
解答 解:A.锌失去电子化合价升高,发生氧化反应作原电池负极,故A正确;
B.锌在负极失电子发生氧化反应,氧气在正极得到电子发生还原反应,所以电池工作时,氧气不是与锌直接化合,故B错误;
C.正极上氧气得电子被还原,电极反应为:$\frac{1}{2}$O2+2e-+2H+═H2O,故C正确;
D.锌在负极失电子发生氧化反应,电极反应为:Zn-2e-+H2O═ZnO+2H+,故D正确;
故选B.
点评 本题考查了原电池知识,为高频考点,侧重于学生的分析能力的考查,注意根据电池反应判断原电池的正负极以及电极反应,注意电解质溶液酸碱性的判断,并结合选项做出判断.


科目:高中化学 来源: 题型:选择题
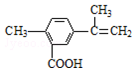
| A. | 在一定条件下,能发生取代、氧化、酯化反应 | |
| B. | 1 mol该物质最多可与2 molNa反应 | |
| C. | 1 mol该物质最多可与4 mol H2发生加成反应 | |
| D. | 1 mol该物质完全氧化最多可消耗13 mol氧气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分别同时滴入等浓度的盐酸,放出气体NaHCO3比Na2CO3快 | |
| B. | 热稳定性Na2CO3<NaHCO3 | |
| C. | 常温时水溶性Na2CO3<NaHCO3 | |
| D. | 相对分子质量Na2CO3<NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
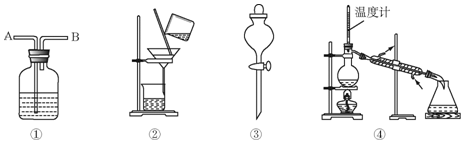
| 选项 | 物质 | 试剂 | 装置 |
| A | C2H6(C2H4) | ① | ① |
| B | 苯(苯酚) | ⑥ | ② |
| C | 苯(苯甲酸) | ⑤ | ④ |
| D | 甲苯(二甲苯) | ③ | ③ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁片、石墨棒,稀硫酸 | B. | 铜片、石墨棒,硝酸银溶液 | ||
| C. | 锌片、铜片,稀盐酸 | D. | 铜片、银片,CuSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、MnO4-、Cl-、SO42- | B. | Na+、AlO2-、Cl-、SO42- | ||
| C. | SO42-、Fe3+、HCO3-、Ba2+ | D. | Mg2+、NO3-、NH4+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
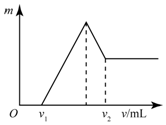 (1)为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,现将100g样品加热使其质量不再变化,其质量变为96.9%,则该样品的纯度(质量分数)是91.6%
(1)为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,现将100g样品加热使其质量不再变化,其质量变为96.9%,则该样品的纯度(质量分数)是91.6%查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com