
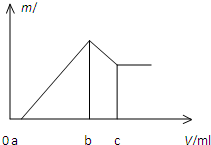 将镁、铝的混合物0.1mol 溶于100mL 2mol/L H2SO4溶液中,然后再滴加1mol/L 的NaOH溶液,沉淀质量m 随加入NaOH溶液的体积V 变化情况如图所示,计算:(1)当a=160mL时,金属混合物中n(Mg)=
将镁、铝的混合物0.1mol 溶于100mL 2mol/L H2SO4溶液中,然后再滴加1mol/L 的NaOH溶液,沉淀质量m 随加入NaOH溶液的体积V 变化情况如图所示,计算:(1)当a=160mL时,金属混合物中n(Mg)=| n |
| V |
| n |
| c |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 0.44mol |
| 1mol/L |
| 0.4mol |
| 1mol/L |


科目:高中化学 来源: 题型:
2- 4 |
| H+ |
| 转换 |
2- 7 |
| Fe2+ |
| 还原 |
| OH- |
| 沉淀 |
2- 4 |
2- 7 |
| 10 |
| 11 |
| A、溶液颜色保持不变,说明上述可逆反应达到平衡状态 |
| B、若用绿矾(FeS04?7H20)(M=278)作还原剂,处理1 L废水,至少需要917.4 g |
| C、常温下转化反应的平衡常数K=1×1014,则转化后所得溶液的pH=6 |
| D、常温下Ksp[Cr(OH)3]=1×10-32,要使处理后废水中的c(Cr3+)降至1×10-5mol/L,应调溶液的pH=5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.65 g |
| B、3.91 g |
| C、5.3 g |
| D、4.23g |
查看答案和解析>>
科目:高中化学 来源: 题型:



查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入AgNO3溶液,生成白色沉淀,再加入稀盐酸,沉淀不溶解,可确定有Cl-存在 |
| B、用洁净铂丝蘸取该溶液在火焰上灼烧,产生黄色火焰,则原溶液中一定含有Na+ |
| C、加入HCl溶液,生成无色无味气体,该气体能使澄清石灰水变浑浊,则原溶液中一定含有CO32- |
| D、加入Ba(NO3)2溶液,生成白色沉淀,加稀盐酸沉淀不溶解,可确定有SO42-存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某温度下在2L密闭容器中加入一定量A,发生以下化学反应:2A(g)═B(g)+C(g);△H=-48.25kJ?mol-1反应过程中B、A的浓度比与时间t有如图所示关系,若测得第15min时c(B)=1.6mol?L-1,下列结论正确的是( )
某温度下在2L密闭容器中加入一定量A,发生以下化学反应:2A(g)═B(g)+C(g);△H=-48.25kJ?mol-1反应过程中B、A的浓度比与时间t有如图所示关系,若测得第15min时c(B)=1.6mol?L-1,下列结论正确的是( )| A、该温度下此反应的平衡常数为3.2 |
| B、A的初始物质的量为4 mol |
| C、反应到达平衡时,放出的热量是193kJ |
| D、反应达平衡时,A的转化率为80% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com