
| A. | 反应进行30s时,正反应速率等于逆反应速率 | |
| B. | 反应进行80s时,逆反应速率大于正反应速率 | |
| C. | 前60 s,以X浓度变化表示的平均反应速率为0.0005mol/(L•s) | |
| D. | 反应进行80s时,X物质的量浓度为0.04mol/L |
分析 经60s达到平衡,生成0.3mol Z,则
2X(g)+Y(g)?Z(g)
开始 1 1 0
转化 0.6 0.3 0.3
平衡 0.4 0.7 0.3
A.反应进行30s时,平衡正向移动;
B.经60s达到平衡,80s时仍为平衡状态;
C.结合v=$\frac{△c}{△t}$计算;
D.结合c=$\frac{n}{V}$计算.
解答 解:经60s达到平衡,生成0.3mol Z,则
2X(g)+Y(g)?Z(g)
开始 1 1 0
转化 0.6 0.3 0.3
平衡 0.4 0.7 0.3
A.反应进行30s时,平衡正向移动,则正反应速率大于逆反应速率,故A错误;
B.经60s达到平衡,80s时仍为平衡状态,则正反应速率等于逆反应速率,故B错误;
C.前60 s,以X浓度变化表示的平均反应速率为$\frac{\frac{0.6mol}{10L}}{60s}$=0.001mol/(L•s),故C错误;
D.反应进行80s时,X物质的量浓度为$\frac{0.4mol}{10L}$=0.04mol/L,故D正确;
故选D.
点评 本题考查化学平衡计算,为高频考点,把握化学平衡三段法、速率及浓度的计算为解答本题关键,侧重分析与应用能力的考查,注意选项B为解答的易错点,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 达到化学平衡时,4v正(O2)=5v逆(NO) | |
| B. | 若单位时间内生成xmolNO的同时,消耗xmol NH3,则反应达到平衡状态 | |
| C. | 化学反应速率关系是:2v正(NH3)=3v正(H2O) | |
| D. | 达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 装置①是电解Na2SO4溶液联合生产硫酸和烧碱示意图,若气体甲,乙的体积比约为1:2,则离子交换膜c、d均为阴离子交换膜,产物丙为硫酸溶液 | |
| B. | 装置②是以肼(N2H4)为燃料的电池装置,a极的反应式:N2H4+4OH--4e-=N2↑+4H2O | |
| C. | 装置③是在待镀铁制品上镀铜的实验装置,电镀过程中电极Ⅱ上Cu2+放电而使溶液中Cu2+浓度逐渐变小 | |
| D. | 装置④是金属牺牲阳极的阴极保护法实验装置,加入K3[Fe(CN)6]溶液后,Fe电极附近会产生蓝色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 氰的分子式为(CN)2,分子中含有3个σ键和4个π键 | |
| B. | 甲醇(CH3OH)分子内的O-C-H键角小于甲醛(HCHO)分子内的O-C-H键角 | |
| C. | 第二周期基态原子未成对电子数与Ni相同且第一电离能最小的元素是氧 | |
| D. | 二氧化硅晶体中最小的环有3个硅原子、3个氧原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 41 | B. | 72 | C. | 113 | D. | 185 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该变化说明原子核在化学反应中也能发生变化 | |
| B. | 该变化遵循质量守恒定律 | |
| C. | 1n是一种电中性粒子 | |
| D. | 对于30P:原子序数=质子数=中子数=核外电子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO42-)>c(NH4+) | |
| B. | 为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH.若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸 | |
| C. | pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色 | |
| D. | 向0.1 mol•L-1的氨水中加入少量硫酸铵固体,则溶液中$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
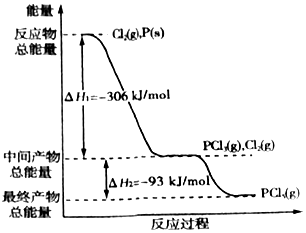 红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据).
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 需要加热方能发生的反应一定是吸热反应 | |
| B. | 放热的反应在常温下一定很容易发生 | |
| C. | 吸热反应在需要在加热条件下才能发生 | |
| D. | 反应是放热还是吸热,必须看反应物和生成物所具有的总能量的相对大小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com