
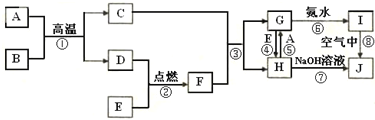
·ÖĪö AŹĒÓĆĶ¾×ī¹ć·ŗµÄ½šŹōµ„ÖŹ£¬BŹĒ³£ĪĀĻĀ³ŹŅŗĢ¬µÄ»ÆŗĻĪļ£¬JŹĒŅ»ÖÖŗģŗÖÉ«³Įµķ£¬ŌņAĪŖFe£¬BĪŖH2O£¬JĪŖFe£ØOH£©3£»EŹĒŅ»ÖÖ»ĘĀĢÉ«µÄĘųĢ壬ŌņEĪŖĀČĘų£®ĢśŌŚøßĪĀĻĀŗĶĖ®ÕōĘų·“Ӧɜ³ÉFe3O4ŗĶH2£¬ĘäÖŠDŗĶĀČĘųæÉ·“Ӧɜ³ÉF£¬FÓėĖÄŃõ»ÆČżĢś·“Ó¦µĆµ½GÓėH£¬ŌņDŹĒH2£¬CŹĒFe3O4£¬FŹĒHCl£¬ŃĪĖįŗĶFe3O4·“Ӧɜ³ÉFeCl2”¢FeCl3£¬HÄÜŗĶĢś·“Ӧɜ³ÉG£¬ĖłŅŌGĪŖFeCl2£¬HĪŖFeCl3£¬ŌņIŹĒFe£ØOH£©2£¬¾Ż“Ė½ā“š£®
½ā“š ½ā£ŗAŹĒÓĆĶ¾×ī¹ć·ŗµÄ½šŹōµ„ÖŹ£¬BŹĒ³£ĪĀĻĀ³ŹŅŗĢ¬µÄ»ÆŗĻĪļ£¬JŹĒŅ»ÖÖŗģŗÖÉ«³Įµķ£¬ŌņAĪŖFe£¬BĪŖH2O£¬JĪŖFe£ØOH£©3£»EŹĒŅ»ÖÖ»ĘĀĢÉ«µÄĘųĢ壬ŌņEĪŖĀČĘų£®ĢśŌŚøßĪĀĻĀŗĶĖ®ÕōĘų·“Ӧɜ³ÉFe3O4ŗĶH2£¬ĘäÖŠDŗĶĀČĘųæÉ·“Ӧɜ³ÉF£¬FÓėĖÄŃõ»ÆČżĢś·“Ó¦µĆµ½GÓėH£¬ŌņDŹĒH2£¬CŹĒFe3O4£¬FŹĒHCl£¬ŃĪĖįŗĶFe3O4·“Ӧɜ³ÉFeCl2”¢FeCl3£¬HÄÜŗĶĢś·“Ӧɜ³ÉG£¬ĖłŅŌGĪŖFeCl2£¬HĪŖFeCl3£¬ŌņIŹĒFe£ØOH£©2£®
£Ø1£©FµÄ»ÆѧŹ½ĪŖHCl£¬¹Ź“š°øĪŖ£ŗHCl£»
£Ø2£©·“Ó¦¢ŁµÄ»Æѧ·“Ó¦·½³ĢŹ½£ŗ3Fe+4H2O£Øg£©$\frac{\underline{\;øßĪĀ\;}}{\;}$Fe3O4+4H2£»
·“Ó¦¢ąµÄ»Æѧ·“Ó¦·½³ĢŹ½£ŗ4Fe£ØOH£©2+2H2O+O2=4Fe£ØOH£©3£¬
¹Ź“š°øĪŖ£ŗ3Fe+4H2O£Øg£©$\frac{\underline{\;øßĪĀ\;}}{\;}$Fe3O4+4H2£»4Fe£ØOH£©2+2H2O+O2=4Fe£ØOH£©3£»
£Ø3£©·“Ó¦¢ŪµÄĄė×Ó·½³ĢŹ½£ŗFe3O4+8H+=2Fe3++Fe2++4H2O£¬
¹Ź“š°øĪŖ£ŗFe3O4+8H+=2Fe3++Fe2++4H2O£»
£Ø4£©¼ų±šFeCl2ČÜŅŗÖŠŃōĄė×ӵķ½·Ø£ŗČ”ŹŹĮæFeCl2ČÜŅŗÓŚŹŌ¹ÜÖŠ£¬ĻČ¼ÓĮņĒč»Æ¼ŲČÜŅŗ£¬Ć»ÓŠĻÖĻó£¬ŌŁ¼ÓĀČĖ®£¬ČÜŅŗ±äŗģ£¬Ö¤Ć÷ŗ¬ÓŠFe2+£¬
¹Ź“š°øĪŖ£ŗČ”ŹŹĮæFeCl2ČÜŅŗÓŚŹŌ¹ÜÖŠ£¬ĻČ¼ÓĮņĒč»Æ¼ŲČÜŅŗ£¬Ć»ÓŠĻÖĻó£¬ŌŁ¼ÓĀČĖ®£¬ČÜŅŗ±äŗģ£¬Ö¤Ć÷ŗ¬ÓŠFe2+£»
£Ø5£©½«FeCl3ČÜŅŗµĪ¼Óµ½·ŠĖ®ÖŠ£¬¼ĢŠų¼ÓČČÖó·Š£¬µĆµ½ĒāŃõ»ÆĢś½ŗĢ壬µĆµ½µÄŅŗĢåŃÕÉ«ĪŖŗģŗÖÉ«£¬
¹Ź“š°øĪŖ£ŗŗģŗÖÉ«£®
µćĘĄ ±¾Ģāæ¼²éĪŽ»śĪļµÄĶʶĻ£¬A”¢B”¢E”¢JĪļÖŹĪŖ½ā“šµÄĶ»ĘĘæŚ£¬ĄūÓĆ×Ŗ»Æ¹ŲĻµĶʶĻ³öø÷ĪļÖŹĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲĢś¼°Ęä»ÆŗĻĪļ×Ŗ»ÆµÄ漲飬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ÓŠŅ»ÖÖŗÖĢśæóÖ÷ŅŖ³É·ÖŹĒFe2O3£¬Ėłŗ¬ŌÓÖŹ²»ČÜÓŚĖ®ŗĶĖį£®Ä³ŃŠ¾æŠŌѧĻ°Š”×éµÄĶ¬Ń§ĆĒĄūÓĆŅ»Š”æéѳʷ£¬½ųŠŠĮĖŅŌĻĀŹµŃ飮
ÓŠŅ»ÖÖŗÖĢśæóÖ÷ŅŖ³É·ÖŹĒFe2O3£¬Ėłŗ¬ŌÓÖŹ²»ČÜÓŚĖ®ŗĶĖį£®Ä³ŃŠ¾æŠŌѧĻ°Š”×éµÄĶ¬Ń§ĆĒĄūÓĆŅ»Š”æéѳʷ£¬½ųŠŠĮĖŅŌĻĀŹµŃ飮²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | æÕĘųÖŹĮæ¼ą²āÖŠµÄPM2.5ŹĒÖø“óĘųÖŠÖ±¾¶Š”ÓŚ»ņµČÓŚ2.5Ī¢Ć×µÄæÅĮ£Īļ£¬Ņ²³ĘæÉČė·ĪæÅĮ£Īļ | |
| B£® | ²ÉÓĆÄÉĆ×TiO2¹ā“„Ć½¼¼Źõ£¬½«Ęū³µĪ²ĘųÖŠµÄNOŗĶCO×Ŗ»ÆĪŖĪŽŗ¦ĘųĢå | |
| C£® | “óĮæÅÅ·ÅSO2»ņCO2¶¼»įµ¼ÖĀĖįÓźµÄŠĪ³É | |
| D£® | ĄūÓĆĢ«ŃōÄÜ”¢³±Ļ«ÄÜ”¢·ēĮ¦·¢µē£¬ŅŌ»ńČ”Ēå½ąÄÜŌ“¼õÉŁĪŪČ¾ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | n1£¾n2 | B£® | n1=n2 | C£® | n2£¾n1 | D£® | c£ØF-£©£¼c£ØCN-£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
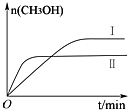 ŃŠ¾æCO2µÄĄūÓƶŌ“Ł½ųµĶĢ¼Éē»įµÄ¹¹½Ø¾ßÓŠÖŲŅŖµÄŅāŅ壮
ŃŠ¾æCO2µÄĄūÓƶŌ“Ł½ųµĶĢ¼Éē»įµÄ¹¹½Ø¾ßÓŠÖŲŅŖµÄŅāŅ壮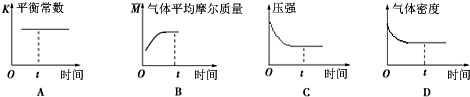
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na2OŗĶNa2O2¾łÄÜÓėH2O·“Ӧɜ³ÉNaOH£¬¹Ź¶žÕ߶¼ŹĒ¼īŠŌŃõ»ÆĪļ | |
| B£® | øł¾Ż·ÖÉ¢ĻµŹĒ·ń¾ßÓŠ¶”“ļ¶ūĻÖĻ󽫷ÖÉ¢Ļµ·ÖĪŖČÜŅŗ”¢½ŗĢåŗĶ×ĒŅŗ | |
| C£® | øł¾ŻĖ®ČÜŅŗÄÜ·ńµ¼µē½«»ÆŗĻĪļ·ÖĪŖµē½āÖŹŗĶ·Ēµē½āÖŹ | |
| D£® | ¼īŠŌŃõ»ÆĪļŅ»¶ØŹĒ½šŹōŃõ»ÆĪļ£¬ĖįŠŌŃõ»ÆĪļ²»Ņ»¶ØŹĒ·Ē½šŹōŃõ»ÆĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś | B£® | ¢Ł¢Ü | C£® | ¢Ś¢Ū | D£® | ¢Ū¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŹµŃéÄŚČŻĪ“ŃĻøń¹ę¶ØŹŌ¼ĮÓĆĮæµÄ£¬æÉČĪŅāČ”ÓĆ | |
| B£® | ŹµŃéŹŅĄļµÄŅ©Ę·³żÕįĢĒ”¢ĘĻĢŃĢĒĶāŅ»Āɲ»µĆĘ·³¢ | |
| C£® | Ņ»°ćĻČÓĆÕōĮóĖ®°ŃPHŹŌÖ½ČóŹŖ£¬Č»ŗóŌŁÉģČėČÜŅŗÖŠ¼ģŃéČÜŅŗµÄĖį¼īŠŌ | |
| D£® | Č”ÓĆ¹ĢĢåŹŌ¼ĮŹ±²»æÉÓĆŹÖÄĆ£¬Ó¦ÓĆÄ÷×Ó»ņŅ©³×Č”ÓĆ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com