
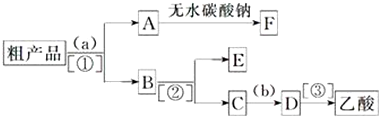
分析 (1)对于液体加热蒸馏,应加入碎瓷片,防止暴沸;
(2)实验室合成乙酸乙酯的实验中浓硫酸作催化剂和吸水剂;
(3)乙酸、乙醇发生酯化反应生成乙酸乙酯;
(4)粗产品乙酸乙酯中含有乙酸与乙醇,用饱和的碳酸钠溶液反应掉乙酸,溶解乙醇,同时降低乙酸乙酯的溶解度,便于溶液分层,乙酸乙酯密度比水小,乙酸乙酯在上层,然后利用分液,乙酸乙酯加入无水碳酸钠吸收其中的水,可得乙酸乙酯;溶液中含有乙醇、碳酸钠、乙酸钠,进行蒸馏可以收集乙醇,向蒸出乙醇的溶液中加入硫酸,可以得到乙酸,再进行蒸馏可以收集乙酸;
(5)得到的乙酸乙酯中加入无水碳酸钠粉末,振荡,除去乙酸乙酯的水份.
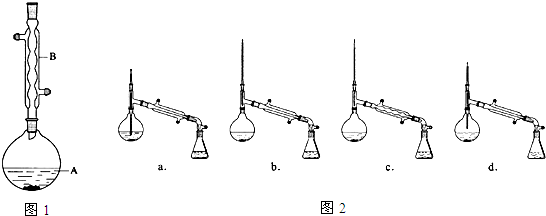
解答 解:(1)对于液体加热蒸馏,应加入碎瓷片,防止暴沸;
故答案为:碎瓷片;防止暴沸;
(2)反应为可逆反应,加入浓硫酸,可起到催化剂的作用,且浓硫酸具有吸水性,有利于反应正向移动,故答案为:催化剂、吸水剂;
(3)乙酸、乙醇发生酯化反应生成乙酸乙酯,反应的化学方程式为CH3CH2OH+CH3COOH$→_{△}^{浓硫酸}$CH3CH2OOCCH3+H2O,
故答案为:CH3CH2OH+CH3COOH$→_{△}^{浓硫酸}$CH3CH2OOCCH3+H2O;
(4)粗产品乙酸乙酯中含有乙酸与乙醇,用饱和的碳酸钠溶液反应掉乙酸,溶解乙醇,同时降低乙酸乙酯的溶解度,便于溶液分层,乙酸乙酯密度比水小,乙酸乙酯在上层,然后利用分液,乙酸乙酯加入无水碳酸钠吸收其中的水,可得乙酸乙酯;溶液中含有乙醇、碳酸钠、乙酸钠,进行蒸馏可以收集乙醇,向蒸出乙醇的溶液中加入硫酸,可以得到乙酸,再进行蒸馏可以收集乙酸;
故答案为:饱和碳酸钠溶液;稀硫酸;萃取分液;蒸馏;蒸馏;乙酸乙酯; 乙醇;
(5)分液得到的乙酸乙酯中含有水分,加入无水碳酸钠粉末,振荡,除去乙酸乙酯的水份.
故答案为:除去乙酸乙酯中的水.
点评 本题考查乙酸乙酯的制备,为高频考点,侧重于学生的分析能力和实验能力的考查,难度不大,注意实验混合液的配制、饱和碳酸钠溶液的作用以及酯化反应的机理,(4)中试剂b选择,由于盐酸易挥发,不能使用盐酸.


科目:高中化学 来源: 题型:选择题
| A. | 少量的CO2通入NaClO溶液中发生反应:NaClO+CO2+H2O=NaHCO3+HClO,说明酸性强弱的顺序为H2CO3>HClO>HCO3- | |
| B. | 金刚石是自然界中硬度最大的物质,不可能与氧气发生反应 | |
| C. | 浓H2SO4具有强氧化性,常温下就能与金属Cu发生剧烈反应 | |
| D. | NO2与H2O 反应的过程中,被氧化的氮原子与被还原的氮原子的个数比为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
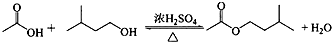
| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 水中溶解性 | |
| 异戊醇 | 88 | 0.8123 | 131 | 微溶 |
| 乙酸 | 60 | 1.0492 | 118 | 溶 |
| 乙酸异戊酯 | 130 | 0.8670 | 142 | 难溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| , | 实验操作 | 预期现象 | 结 论 |
| 验证猜想I] | 步骤①:取少量0.01mol/L 酸性KMnO4溶液,滴入所得溶液中 | 溶液紫红色褪去 | 含有Fe2+ |
| 步骤②:另取少量所得溶液,滴加KI溶液和淀粉溶液 | 溶液不变为蓝色 | 不含Fe3+ | |
| 验证猜想Ⅱ | 将所得气体通入如下装置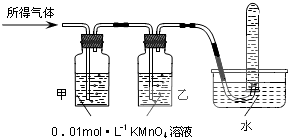 | 甲中KMnO4溶液褪色,乙中KMnO4溶液颜色不变,试管中收集到气体 | 含有两种气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
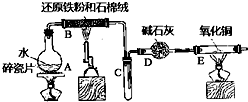 某实验小组利用下图所列装置进行“铁与水蒸气反应”的实验,并利用产物进一步制取FeCl3•6H2O晶体.(图中夹持及尾气处理装置均已略去)请回答下列问题:
某实验小组利用下图所列装置进行“铁与水蒸气反应”的实验,并利用产物进一步制取FeCl3•6H2O晶体.(图中夹持及尾气处理装置均已略去)请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
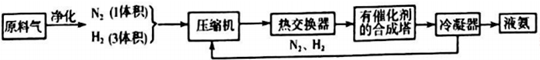
| 气体 | CO | H2 | N2 | O2 |
| 体积(L) | 25 | 60 | 15 | 2.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com