
| A. | 根据同周期元素的第一电离能变化趋势,推出Al的第一电离能比Mg大 | |
| B. | 根据较强酸可以制取较弱酸的规律,推出CO2通入NaClO溶液中能生成HClO | |
| C. | 根据溶液的pH与溶液酸碱性的关系,推出pH=6.8的溶液一定显酸性 | |
| D. | 根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7 |
分析 A.Mg的3s电子全满,为稳定结构;
B.CO2通入NaClO溶液中,发生强酸制取弱酸的反应;
C.温度未知,不能确定中性溶液的pH;
D.F无正价.
解答 解:A.Mg的3s电子全满,为稳定结构,则Al的第一电离能比Mg小,故A错误;
B.CO2通入NaClO溶液中,发生强酸制取弱酸的反应,则生成HClO,故B正确;
C.温度未知,不能确定中性溶液的pH,若为常温可知pH=6.8的溶液显酸性,故C错误;
D.F无正价,除F外卤族元素最高正价是+7,故D错误;
故选B.
点评 本题考查元素周期律和周期表,为高频考点,把握元素的位置、性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意元素的特性,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 冬天,5%H2O2溶液分解 | B. | 冬天,MnO2与5%H2O2溶液混合 | ||
| C. | 夏天,5%H2O2溶液分解 | D. | 夏天,MnO2与5%H2O2溶液混合 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 药物名称 | 胃舒平(复方氢氧化铝) |
| 有效成分 | 氢氧化铝和三硅酸镁 |
| 不良反应 |  |
| 实验步骤 | (1)将药片3-4片研碎,向样品中滴加过量盐酸,过滤,得到澄清溶液; (2)向滤液中滴加NaOH溶液,观察是否出现白色沉淀; (3)如有白色沉淀生成,继续滴加NaOH溶液,观察白色沉淀是否溶解. |
| 结 论 | 胃舒平中含有氢氧化铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝合金的大量使用,归功于人们用电解法从氧化铝中获取铝 | |
| B. | 铜的活动性比铁弱,故在海轮外壳装铜块减缓海轮腐蚀 | |
| C. | 用电镀厂的废水中直接灌溉农田,可提高水的利用率 | |
| D. | 甲醛溶液具有杀菌消毒的能力,故能用甲醛溶液浸泡食品 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. 的系统命名为3-甲基-戊烷.
的系统命名为3-甲基-戊烷. .
. 中,共平面的碳原子最多有13个,共直线的原子最多有5个,该分子中有4种不同化学环境的H原子.
中,共平面的碳原子最多有13个,共直线的原子最多有5个,该分子中有4种不同化学环境的H原子.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
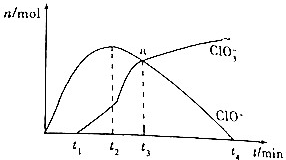 工业上把Cl2通入冷NaOH溶液中制得漂白液(主要成分为NaClO),某化学小组在一定温度下将氯气缓缓通入NaOH溶液,模拟实验得到ClO-、ClO${\;}_{3}^{-}$的物质的量(mol)与反应时间t(min)的关系如图所示.下列说法错误的是( )
工业上把Cl2通入冷NaOH溶液中制得漂白液(主要成分为NaClO),某化学小组在一定温度下将氯气缓缓通入NaOH溶液,模拟实验得到ClO-、ClO${\;}_{3}^{-}$的物质的量(mol)与反应时间t(min)的关系如图所示.下列说法错误的是( )| A. | 参加反应所需要NaOH与氯气的物质的量之比一定为2:1 | |
| B. | a点时溶液中n(NaCl):n(NaClO3):n(NaClO)=6:1:1 | |
| C. | t2~t4min,ClO-的物质的量下降的原因可能是3ClO-═2Cl-+ClO${\;}_{3}^{-}$ | |
| D. | 使用漂白液时,为了增强漂白效果,可以向漂白液中加入浓盐酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com