
| A. | 混合气体一定是CH4和C2H4 | |
| B. | 混合气体中一定有CH4,可能含有C2H4 | |
| C. | 混合气体中一定含有CH4,可能含有C2H6 | |
| D. | 混合气体中可能含有C2H2 |
分析 反应生成的3.6g水的物质的量为:n(H2O)=$\frac{3.6g}{18g/mol}$=0.2mol,即0.1mol混合烃完全燃烧生成0.16molCO2和0.2molH2O,根据元素守恒,则混合烃的平均分子式为C1.6H4,而碳原子数小于1.6的只有甲烷,则一定含有甲烷,然后根据平均分子式进行判断.
解答 解:n(H2O)=$\frac{3.6g}{18g/mol}$=0.2mol,即0.1mol混合烃完全燃烧生成0.16molCO2和0.2molH2O,根据元素守恒,混合烃的平均分子式为C1.6H4;
烃中C原子数小于1.6的只有CH4,则混合气体中一定含有CH4,由于CH4分子中含4个H原子,则另一种烃分子中一定含4个H原子,且其C原子数大于1.6,故可能是C2H4或C3H4,
A.根据以上分析可知,混合气体中一定含有CH4,可能存在C2H4,故A错误;
B.混合气体中一定含有CH4,可能含有C2H4,即不一定含有乙烯,故B正确;
C.由于氢原子平均为4,则另一种烃分子中一定含4个H原子,所以混和气体中一定没有C2H6,故C错误;
D.混合烃的平均分子式为:C1.6H4,烃中C原子数小于1.6的只有CH4,则一定含有CH4,CH4分子中含4个H原子,故另一种分子中一定含4个H原子,则一定没有乙炔,故D错误;
故选B.
点评 本题考查了混合物反应的计算,题目难度中等,解答关键是能够正确分析有机物完全燃烧生成的CO2和H2O的物质的量关系,注意掌握平均分子式法在确定有机物组成中的应用方法.


科目:高中化学 来源: 题型:选择题
| A. | 集中处理废旧电池,以防止重金属污染环境 | |
| B. | 海产品中加入大量甲醛以延长保鲜期 | |
| C. | 食用蔬菜水果可以补充人体所需维生素 | |
| D. | 使用加碘盐,可预防因缺碘引起的甲状腺肿大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁和铝 | B. | 锌和铝 | C. | 镁和铝 | D. | 铜和铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
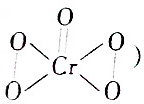 )
)| A. | ①②③ | B. | ② | C. | ③ | D. | 都不是 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况时11.2LO2的质量为32g | B. | 16O的相对原子质量为32 | ||
| C. | 44gCO2和28gCO含有相同的分子数 | D. | 标准状况时44gCO2的体积是22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| A元素原子的核外p电子总数比s电子总数少1 |
| B原子核外所有p轨道全满或半满 |
| C元素的主族序数与周期数的差为4 |
| D是前四周期中电负性最小的元素 |
| E在周期表的第十一列 |
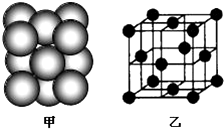
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
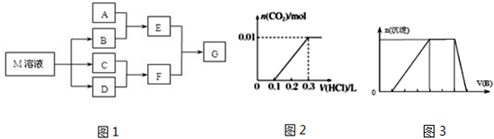
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com