
”¾ĢāÄæ”æ½«Ć¾”¢ĀĮµÄ»ģŗĻĪļ¹²0.2mol£¬ČÜÓŚ200mL 4molL©1µÄŃĪĖįČÜŅŗÖŠ£¬Č»ŗóŌŁµĪ¼Ó2molL©1µÄNaOHČÜŅŗ£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ČōŌŚµĪ¼ÓNaOHČÜŅŗµÄ¹ż³ĢÖŠ£¬³ĮµķÖŹĮæm Ėę¼ÓČėNaOHČÜŅŗµÄĢå»żV±ä»ÆĒéæöČēĶ¼ĖłŹ¾£®µ±V1=160mLŹ±£¬Ōņ½šŹō·ŪÄ©ÖŠn £ØAl£©=mol 
£Ø2£©0”«V1¶Ī·¢ÉśµÄ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£»
£Ø3£©ČōŌŚµĪ¼ÓNaOHČÜŅŗµÄ¹ż³ĢÖŠ£¬ÓūŹ¹Mg2+”¢Al3+øÕŗĆ³ĮµķĶźČ«£¬ŌņµĪČėNaOHČÜŅŗµÄĢå»żV£ØNaOH£©=mL£»
£Ø4£©ČōĆ¾”¢ĀĮµÄ»ģŗĻĪļČŌĪŖ0.2mol£¬ĘäÖŠĆ¾·ŪµÄĪļÖŹµÄĮæ·ÖŹżĪŖa£¬øÄÓĆ200mL 4molL©1µÄĮņĖįČܽā“Ė»ģŗĻĪļŗó£¬ŌŁ¼ÓČė840mL 2molL©1µÄNaOHČÜŅŗ£¬ĖłµĆ³ĮµķÖŠĪŽAl£ØOH£©3 £¬ ŌņaµÄȔֵ·¶Ī§ĪŖ £®
”¾“š°ø”æ
£Ø1£©0.08
£Ø2£©H++OH©=H2O
£Ø3£©400
£Ø4£©0.6”Üa£¼1
”¾½āĪö”æ½ā£ŗ£Ø1£©µ±V1=160mLŹ±£¬“ĖŹ±£¬ČÜŅŗŹĒMgCl2”¢AlCl3ŗĶNaClµÄ»ģŗĻŅŗ£¬ ÓÉNa+Ąė×ÓŹŲŗćæÉÖŖ£¬n£ØNaCl£©=n£ØNa+£©=n£ØNaOH£©=0.16L”Į2mol/L=0.32mol£¬
200mL 4molL©1µÄŃĪĖįČÜŅŗÖŠŗ¬ÓŠĀČ»ÆĒāµÄĪļÖŹµÄĮæĪŖ£ŗ4mol/L”Į0.2L=0.8mol£¬
Éč»ģŗĻĪļÖŠŗ¬ÓŠMgCl2xmol”¢AlCl3ĪŖymol£¬Ōņ£ŗ
øł¾ŻMgŌ×Ó”¢AlŌ×ÓŹŲŗćÓŠ£ŗx+y=0.2£¬
øł¾ŻCl©Ąė×ÓŹŲŗćÓŠ£ŗ2x+3y=0.8©0.32=0.48£¬
ĮŖĮ¢·½³Ģ½āµĆ£ŗx=0.12”¢y=0.08£¬
ĖłŅŌ½šŹō·ŪÄ©ÖŠ£ŗn£ØMg£©=0.12mol”¢n£ØAl£©=y=0.08mol£¬
¹Ź“š°øĪŖ£ŗ0.08£»£Ø2£©0”«V1¶Ī£¬µĪČėĒāŃõ»ÆÄĘČÜŅŗŗóƻӊɜ³É³Įµķ£¬ĖµĆ÷ŃĪĖį¹żĮ棬µĪČėµÄĒāŃõ»ÆÄĘÓėĀČ»ÆĒā·“Ӧɜ³ÉĀČ»ÆÄĘŗĶĖ®£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗH++OH©=H2O£¬
¹Ź“š°øĪŖ£ŗH++OH©=H2O£»£Ø3£©µ±ČÜŅŗÖŠMg2+”¢Al3+Ē”ŗĆ³ĮµķĶźČ«Ź±£¬“ĖŹ±£¬ČÜŅŗŹĒNaClČÜŅŗ£¬øł¾ŻCl©Ąė×ÓŗĶNa+Ąė×ÓŹŲŗćÓŠ£ŗn£ØNa+£©=n£ØNaCl£©=£ØHCl£©=4mol/L”Į0.2L=0.8mol£¬
ĖłŅŌŠčŅŖ¼ÓČėĒāŃõ»ÆÄĘČÜŅŗĢå»żĪŖ£ŗV£ØNaOH£©= ![]() =0.4L=400mL£¬
=0.4L=400mL£¬
¹Ź“š°øĪŖ£ŗ400£»£Ø4£©ÓÉÓŚĪŖ½šŹō»ģŗĻĪļ£¬Ōņa£¼1£¬AlµÄĪļÖŹµÄĮæĪŖ£ŗ0.2£Ø1©a£©mol£¬·“Ó¦ŗóµÄ»ģŗĻČÜŅŗ£¬ŌŁ¼ÓČė840mL 2molL©1µÄNaOHČÜŅŗ£¬ĖłµĆ³ĮµķÖŠĪŽAl£ØOH£©3 £¬ ŌņČÜÖŹĪŖĮņĖįÄĘ”¢Ę«ĀĮĖįÄĘ£¬øł¾ŻĀĮŌŖĖŲŹŲŗćæÉÖŖ£ŗn£ØNaAlO2£©=0.2£Ø1©a£©mol£¬
øł¾ŻÄĘĄė×ÓŹŲŗć£¬Ó¦Āś×ć£ŗn£ØNaOH£©”Ż2n£ØNa2SO4£©+n£ØNaAlO2£©£¬¼“0.84”Į2”Ż2”Į0.2”Į4+0.2£Ø1©a£©£¬
½āµĆ£ŗa”Ż0.6£¬
ĖłŅŌaµÄȔֵ·¶Ī§ĪŖ£ŗ¹Ź0.6”Üa£¼1£¬
¹Ź“š°øĪŖ£ŗ0.6”Üa£¼1£®
£Ø1£©øł¾ŻĶ¼ĻóæÉÖŖ£¬ŌŚµĪ¼ÓNaOHČÜŅŗµ½Ģå»żV1=160mL¹ż³ĢÖŠ£¬Ć»ÓŠ³ĮµķÉś³É£¬ĖµĆ÷ŃĪĖįÓŠŹ£Óą£¬µĪ¼ÓµÄNaOHÓĆÓŚÖŠŗĶŹ£ÓąŃĪĖį£¬V1=160mLŹ±£¬Ź£ÓąµÄHClÓėµĪ¼ÓµÄNaOHĒ”ŗĆĶźČ«·“Ó¦£¬ČÜŅŗŹĒMgCl2”¢AlCl3ŗĶNaCl»ģŗĻŅŗ£¬øł¾ŻMgŌ×Ó”¢AlŌ×Ó”¢Cl©Ąė×Ó”¢Na+Ąė×ÓŹŲŗć£¬ĮŠ·½³ĢĒóĖćn£ØAl£©£»£Ø2£©0”«V1¶ĪµĪČėµÄĒāŃõ»ÆÄĘČÜŅŗÓėŹ£ÓąµÄĀČ»ÆĒā·“Ӧɜ³ÉĀČ»ÆÄĘŗĶĖ®£»£Ø3£©µ±ČÜŅŗÖŠMg2+”¢Al3+Ē”ŗĆ³ĮµķĶźČ«Ź±£¬¼“³Įµķ“ļµ½×ī“óÖµ£¬“ĖŹ±£¬ČÜŅŗŹĒNaClČÜŅŗ£¬øł¾ŻCl©Ąė×ÓŗĶNa+Ąė×ÓŹŲŗćÓŠn£ØNa+£©=n£ØNaCl£©=£ØHCl£©Ēó³ön£ØNaOH£©£¬ŌŁĄūÓĆV= ![]() ¼ĘĖćµĪČėNaOHČÜŅŗµÄĢå»ż£»£Ø4£©·“Ó¦ŗóµÄ»ģŗĻČÜŅŗ£¬ŌŁ¼Ó840mL 2molL©1µÄNaOHČÜŅŗ£¬ĖłµĆ³ĮµķÖŠĪŽAl£ØOH£©3 £¬ ČÜÖŹĪŖĮņĖįÄĘ”¢Ę«ĀĮĖįÄĘ£¬ÓÉÓŚĪŖ½šŹō»ģŗĻĪļ£¬Ōņa£¼1£¬øł¾ŻÄĘĄė×ÓŹŲŗć£¬Ó¦Āś×ćn£ØNaOH£©”Ż2n£ØNa2SO4£©+n£ØNaAlO2£©£¬øł¾ŻĀĮŌŖĖŲŹŲŗćÓĆa±ķŹ¾³ön£ØNaAlO2£©£¬¾Ż“ĖČ·¶ØaµÄȔֵ·¶Ī§£®
¼ĘĖćµĪČėNaOHČÜŅŗµÄĢå»ż£»£Ø4£©·“Ó¦ŗóµÄ»ģŗĻČÜŅŗ£¬ŌŁ¼Ó840mL 2molL©1µÄNaOHČÜŅŗ£¬ĖłµĆ³ĮµķÖŠĪŽAl£ØOH£©3 £¬ ČÜÖŹĪŖĮņĖįÄĘ”¢Ę«ĀĮĖįÄĘ£¬ÓÉÓŚĪŖ½šŹō»ģŗĻĪļ£¬Ōņa£¼1£¬øł¾ŻÄĘĄė×ÓŹŲŗć£¬Ó¦Āś×ćn£ØNaOH£©”Ż2n£ØNa2SO4£©+n£ØNaAlO2£©£¬øł¾ŻĀĮŌŖĖŲŹŲŗćÓĆa±ķŹ¾³ön£ØNaAlO2£©£¬¾Ż“ĖČ·¶ØaµÄȔֵ·¶Ī§£®


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĆę·ŪµÄÉś²ś³µ¼ä±ŲŠėŃĻ½ūĪüŃĢ£¬Ö÷ŅŖµÄÄæµÄŹĒ
A.±ÜĆāŃĢ³¾ŌÓČėĆę·ŪB.±£»¤¹¤ČĖ½”æµ
C.·ĄÖ¹ĪŪČ¾»·¾³D.·ĄÖ¹·¢Éś±¬ÕØ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”抔Ć÷ŅņĢåČȱ·¦Ä³ÖÖĪ¬ÉśĖŲ£¬»¼ĮĖŅ¹Ć¤Ö¢£¬Ķ¬Ń§ĆĒĘß×ģ°ĖÉąµŲøųĖūĢį¹©²¹³äøĆĪ¬ÉśĖŲµÄŹ³Ę×”£ĻĀĮŠŹ³Ę·¶Ō²¹³äĪ¬ÉśĖŲÖĪĮĘĖūµÄŅ¹Ć¤Ö¢Ć»ÓŠĆ÷ĻŌ×÷ÓƵďĒ
A.ÓćøĪÓĶB.Ė®¹ūC.¶ÆĪļøĪŌąD.¶¹ÖĘĘ·
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø £©
A.ĖÜĮĻŌŚ×ŌČ»Ģõ¼žĻĀ²»Ņ×·Ö½ā£¬æÉŌģ³É°×É«ĪŪČ¾
B.ŗĻ³ÉĻĖĪ¬µÄÖ÷ŅŖŌĮĻæÉŅŌŹĒŹÆÓĶ”¢ĢģČ»Ęų”¢ĆŗŗĶÅ©ø±²śĘ·
C.ĢģČ»Ļš½ŗµÄŠŌÖŹŗÜĪČ¶Ø£¬ŌŚæÕĘų”¢ČÕ¹ā×÷ÓĆĻĀŅ²²»»įĄĻ»Æ
D.ĖÜĮĻ”¢ŗĻ³ÉĻĖĪ¬ŗĶŗĻ³ÉĻš½ŗ¶¼ŹĒøß·Ö×Ó»ÆŗĻĪļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠø÷×éĖ³ŠņµÄÅÅĮŠ²»ÕżČ·µÄŹĒ
A. ČČĪČ¶ØŠŌ£ŗHCl£¾H2S£¾PH3 B. ČōĄė×Ó°ė¾¶£ŗR2£>M+£¬ŌņŌ×ÓŠņŹżŅ»¶Ø£ŗR >M
C. ĖįŠŌĒæČõ£ŗH2SiO3£¼H2CO3£¼CH3COOH D. ČŪµć£ŗ½šøÕŹÆ£¾Ź³ŃĪ£¾øɱł
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠA”¢B”¢C”¢D”¢EĪåÖÖ¶ĢÖÜĘŚŌŖĖŲ£¬ŅŃÖŖ:¢ŁC+”¢D3+¾łÓėEµÄĘųĢ¬Ēā»ÆĪļ·Ö×Óŗ¬ÓŠĻąĶ¬µÄµē×ÓŹż;A2-”¢B-ÓėBµÄĘųĢ¬Ēā»ÆĪļ·Ö×Óŗ¬ÓŠĻąĶ¬µÄµē×ÓŹż;¢ŚAµ„ÖŹŌŚæÕĘųÖŠČ¼ÉÕ²śÉśĘųĢåR;¢ŪBµÄĘųĢ¬Ēā»ÆĪļÓėEµÄĘųĢ¬Ēā»ÆĪļĻąÓöŹ±ÓŠ°×ŃĢÉś³É”£
Ēė»Ų“šĻĀĮŠĪŹĢā:
(1)ŌŖĖŲAŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆŹĒ__________
(2)A”¢B”¢C”¢DµÄ¼ņµ„Ąė×Ó°ė¾¶“ӓ󵽊”Ė³ŠņĪŖ______________(ÓĆĄė×Ó·ūŗűķŹ¾)
(3)BµÄĘųĢ¬Ēā»ÆĪļÓėEµÄĘųĢ¬Ēā»ÆĪļĻąÓöŹ±Éś³É°×ŃĢµÄµē×ÓŹ½ĪŖ_________£¬ĘäÖŠĖłŗ¬»Æѧ¼üĄąŠĶĪŖ_____________
(4)DµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļÓėCµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ_____
(5)AŌŖĖŲŗĶBŌŖĖŲŅŌŌ×ÓøöŹż±Č1:1ŠĪ³É»ÆŗĻĪļQ£¬QµÄ½į¹¹Ź½ĪŖ________
¼ŗÖŖQŹĒÖÖ»ĘÉ«ÓĶדŅŗĢ壬³£ĪĀĻĀÓöĖ®Ņ×·“Ó¦£¬²śÉśRĘųĢ壬Ņ×ČÜŅŗ³öĻÖ»ė×Ē£¬ĒėŠ“QÓėĖ®·“Ó¦µÄ»Æѧ·½³ĢŹ½___________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŃĒĻõĖįÄĘ£ØÓŠ¶¾ŠŌ£¬ŹŠ³”ÉĻŗÜŅ×ÓėŹ³ŃĪ»ģĻż£©ŹĒŅ»ÖÖ³£¼ūµÄ¹¤ŅµÓĆŃĪ£¬¹ć·ŗÓĆÓŚĪļÖŹŗĻ³É”¢½šŹō±ķĆꓦĄķµČ£¬ĪļĄķŠŌÖŹÓėNaCl¼«ĪŖĻąĖĘ”£Ļą¹Ų»ÆѧŠŌÖŹČēÓŅĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
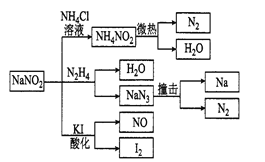
A. NaNO2ĪČ¶ØŠŌ“óÓŚNH4 NO
B. NaNO2ÓėN2 H4·“Ó¦ÖŠ£¬NaNO2ŹĒŃõ»Æ¼Į
C. æÉÓĆKI-µķ·ŪŹŌÖ½ŗĶŹ³“×¼ų±šNaNO2ŗĶNaCl
D. ·Ö½āNaN3ŃĪĆæ²śÉś1 mol N2×ŖŅĘ6 mol eŅ»
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫ČéĒåµ°°×”¢µķ·Ū”¢Īøµ°°×Ćø”¢ĶŁŅŗµķ·ŪĆøŗĶŹŹĮæĖ®»ģŗĻ×°ČėŅ»øöČŻĘ÷ÄŚ£¬µ÷ÕūpHÖĮ2£®0£¬±£“ęÓŚ37”ęµÄĖ®ČܹųÖŠ£¬¹żŅ»¶ĪŹ±¼äŗó£¬ČŻĘ÷ÄŚŹ£ÓąµÄĪļÖŹŹĒ
A£®µķ·Ū”¢Īøµ°°×Ćø”¢¶ąėÄ”¢Ė®
B£®ĶŁŅŗµķ·ŪĆø”¢µķ·Ū”¢Īøµ°°×Ćø”¢Ė®
C£®ĶŁŅŗµķ·ŪĆø”¢Īøµ°°×Ćø”¢¶ąėÄ”¢Ė®
D£®ĶŁŅŗµķ·ŪĆø”¢ĀóŃæĢĒ”¢Īøµ°°×Ćø”¢¶ąėÄ”¢Ė®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij»ÆѧŠĖȤŠ”×éŃ”ÓĆĻĀĮŠ×°ÖĆŗĶŅ©Ę·ÖĘČ”“æ¾»ŅŅČ²²¢½ųŠŠÓŠ¹ŲŅŅČ²ŠŌÖŹµÄĢ½¾æ£¬ŹŌ»Ų“šĻĀĮŠĪŹĢā”£
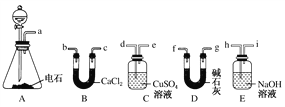
£Ø1£©AÖŠÖĘČ”ŅŅČ²µÄ»Æѧ·½³ĢŹ½ĪŖ_________________________________”£
£Ø2£©ÖĘŅŅČ²Ź±£¬ŠżæŖ·ÖŅŗĀ©¶·µÄ»īČū£¬Ź¹Ė®ĀżĀżµĪĻĀµÄŌŅņŹĒ_________________”£
£Ø3£©ÓƵēŹÆÖʵƵÄŅŅČ²ÖŠ³£ŗ¬ÓŠH2S”¢PH3µČŌÓÖŹ£¬³żČ„ŌÓ֏ӦєÓĆ________(ĢīŠņŗÅ£¬ĻĀĶ¬)×°ÖĆ£¬øÉŌļŅŅČ²×īŗĆŃ”ÓĆ________×°ÖĆ”£
£Ø4£©ĪŖĮĖĢ½¾æŅŅČ²ÓėHBr·¢Éś¼Ó³É·“Ó¦ŗóµÄÓŠ¹Ų²śĪļ£¬½ųŠŠŅŌĻĀŹµŃé£ŗ
“æ¾»ŅŅČ²Ęų![]() »ģŗĻŅŗ
»ģŗĻŅŗ![]() ÓŠ»ś»ģŗĻĪļ¢ń
ÓŠ»ś»ģŗĻĪļ¢ń![]() »ģŗĻŅŗ
»ģŗĻŅŗ![]() ÓŠ»ś»ģŗĻĪļ¢ņ
ÓŠ»ś»ģŗĻĪļ¢ņ
¢Ł²Ł×÷bµÄĆū³ĘŹĒ________£»
¢ŚÓŠ»ś»ģŗĻĪļ¢ńæÉÄÜŗ¬ÓŠµÄĪļÖŹŹĒ________(Š“½į¹¹¼ņŹ½)”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com