

| A. | a为电源的负极 | |
| B. | 负极反应方程式为:Ag-e-+Cl-═AgCl | |
| C. | 阴极的电极反应式为2HSO3-+2H++2e-═S2O42-+2H2O | |
| D. | 当电路中转移电子的物质的量为5×10-5 mol时,进入传感器的SO2为1.12 mL |
分析 A、与b电极连接的电解池的电极上发生HSO3-变化为S2O42-,硫元素化合价降低发生还原反应,判断为阴极;
B、与电源a极相连的电极为电解池的阳极;
C、阴极的电极反应为HSO3-变化为S2O42-,依据电荷守恒和原子守恒书写电极反应判断;
D、温度和压强不知不能计算气体体积.
解答 解:A、与b电极连接的电解池的电极上发生HSO3-变化为S2O42-,硫元素化合价降低发生还原反应,判断为阴极,b电极为原电池的负极,故A错误;
B、与电源a极相连的电极为电解池的阳极,电极反应式 Ag-e-+Cl-═AgCl,故B错误;
C、阴极的电极反应为HSO3-变化为S2O42-,依据电荷守恒和原子守恒书写电极反应为2HSO3-+2H++2e-═S2O42-+2H2O,故C正确;
D、温度和压强不知不能计算气体体积,故D错误.
故选C.
点评 本题考查了原电池、电解池原理的分析判断,主要是电极分析,掌握基础是关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 该反应中硝酸表现了氧化性和酸性 | |
| B. | 硝酸铵既是氧化产物又是还原产物 | |
| C. | 该反应中被氧化与被还原的物质的质量比为260:63 | |
| D. | 该反应中电子转移数目为8e- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
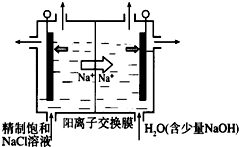 二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.
二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用一种原子制造出另一种或几种原子 | |
| B. | 碳酸氢铵受热分解 | |
| C. | 蓝矾加热后变为白色固体 | |
| D. | 电解水生成氢气和氧气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4L O2一定含有NA个氧分子 | |
| B. | 1mol H2的质量只有在标准状况下才约为2g | |
| C. | 标准状况下,18g水的体积为22.4L | |
| D. | 1mol H2和O2的混合气体在标准状况下的体积约为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
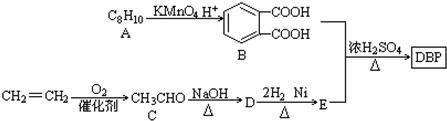
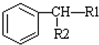 $\stackrel{KMnO_{2}H+}{→}$
$\stackrel{KMnO_{2}H+}{→}$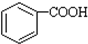
 (-R1、-R2表示氢原子或烃基)
(-R1、-R2表示氢原子或烃基)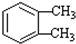 ,D→E的反应类型加成(或还原)反应.
,D→E的反应类型加成(或还原)反应.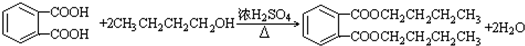 .
.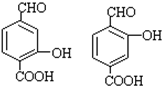 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(Na+)=1mol/L,c(Cl-)=1mol/L,c(Ca2+)=2mol/L,c(ClO4-)=4mol/L | |
| B. | c(K+)=1mol/L,c(Mg2+)=1mol/L,c(Cu2+)=1mol/L,c(NO${\;}_{3}^{-}$)=4mol/L | |
| C. | c(OH-)=1mol/L,c(SO${\;}_{4}^{2-}$)=1mol/L,c(NH${\;}_{4}^{+}$)=6mol/L,c(HCO${\;}_{3}^{-}$)=1mol/L | |
| D. | c(Al3+)=1mol/L,c(SO${\;}_{4}^{2-}$)=1mol/L,c(OH-)=2mol/L,c(Na+)=2mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com