
| A. | 只有②③ | B. | 只有③④ | C. | 只有①③ | D. | 只有①④ |
分析 ①由乙烯、氢气制取乙烷为加成反应、由乙烷、溴(气体)制溴乙烷为取代反应;
②乙烯使溴水褪色发生加成反应、乙炔使酸性高锰酸钾水溶液褪色发生氧化反应;
③由乙醇、乙酸制乙酸乙酯为取代反应、由甘氨酸制得二肽为取代反应;
④由乙烯、氯化氢制取氯乙烷为加成反应、由乙炔、氯化氢制取氯乙烯为加成反应.
解答 解:①由乙烯、氢气制取乙烷为加成反应、由乙烷、溴(气体)制溴乙烷为取代反应,反应类型不同,故不选;
②乙烯使溴水褪色发生加成反应、乙炔使酸性高锰酸钾水溶液褪色发生氧化反应,反应类型不同,故不选;
③由乙醇、乙酸制乙酸乙酯为取代反应、由甘氨酸制得二肽为取代反应,反应类型相同,故选;
④由乙烯、氯化氢制取氯乙烷为加成反应、由乙炔、氯化氢制取氯乙烯为加成反应,反应类型相同,故选;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应等为解答的关键,侧重有机反应类型的判断及分析与应用能力的考查,题目难度不大.


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:解答题
| 压强(Pa) | 4×105 | 6×105 | 10×105 | 20×105 |
| D的浓度(mol/L) | 0.085 | 0.126 | 0.200 | 0.440 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解质AgNO3溶液的浓度变为0.08mol/L | |
| B. | 阳极上产生112mLO2(标况) | |
| C. | 转移1.204×1022个电子 | |
| D. | 反应中有0.01mol的Ag被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向溶液中加入0.245g Cu(OH)2 | B. | 向溶液中加入0.31gCuCO3 | ||
| C. | 向溶液中加入0.0025 molH2SO4 | D. | 向溶液中加入0.2gCuO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
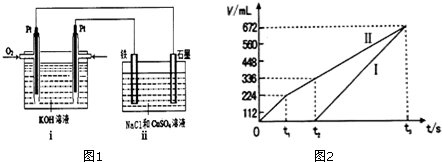
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 气体W为氧气 | |
| B. | b极与电源的正极相连 | |
| C. | 离子交换膜c为阳离子交换膜 | |
| D. | a极的电极反应为SO2+2H2O-2e-=SO42-+4H+. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

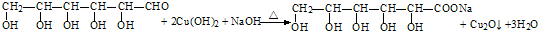
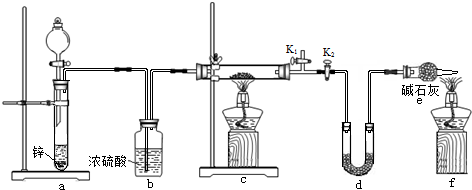
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
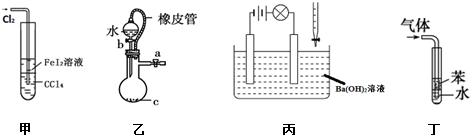
| A. | 甲装置可以用于比较Fe3+、I2、Cl2的氧化性强弱 | |
| B. | 乙装置中打开分液漏斗活塞,水不能顺利流下,说明该装置气密性良好 | |
| C. | 丙装置中若向Ba(OH)2溶液中逐滴加入硫酸溶液直至过量,灯光会由亮变暗至熄灭后又逐渐变亮 | |
| D. | 丁装置不能用于吸收HCl气体及防倒吸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-═Cl2↑ | |
| B. | NaHS水解:HS-+H2O?S2-+H3O+ | |
| C. | 在碱性介质中,氢氧燃料电池的负极反应式为:O2+4e-═2O2- | |
| D. | NaHCO3电离:NaHCO3?Na++HCO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com