
| A. | $\frac{m}{A+16}$(A-n+8)mol | B. | $\frac{m}{A+16}$(A-n+10)mol | C. | (A-n+2)mol | D. | $\frac{m}{A}$(A-n+6)mol |
分析 阳离子R2+的核内中子数为n,质量数为A,所以质子数为A-n,该离子的相对原子质量在数值上等于其质量数;该离子带2个单位正电荷,所以其氧化物的化学式为RO,该氧化物的摩尔质量为(A+16)g/mol,根据n=$\frac{m}{M}$计算mg该氧化物的物质的量,一个氧化物分子中含有(A-n+8)个质子,据此计算.
解答 解:阳离子R2+的核内中子数为n,质量数为A,所以质子数为A-n,
该离子带2个单位正电荷,所以其氧化物的化学式为RO,该氧化物的摩尔质量为(A+16)g/mol,
m g 它的氧化物的物质的量为$\frac{mg}{(A+16)g/mol}$=$\frac{m}{A+16}$mol,
一个氧化物分子中含有(A-N+8)个质子,所以mg 它的氧化物中所含质子的物质的量为=$\frac{m}{A+16}$mol×(A-n+8)=$\frac{m}{A+16}$×(A-n+8)mol,
故选A.
点评 本题考查物质的量有关计算、原子构成,侧重考查微粒数目计算,关键是理解质子数、中子数、质量数之间的关系.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 原子核内有10个中子的氧原子188O | B. | 乙烯的结构简式为:C2H4 | ||
| C. | CH4分子的比例模型: | D. | CO2的电子式: |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 甘油加水作护肤剂 | |
| B. | 明矾净水 | |
| C. | 蒸鱼时加入少量的料酒和食醋可减少腥味、增加香味 | |
| D. | 烧菜用过的铁锅,放置一段时间后会出现红棕色斑迹 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
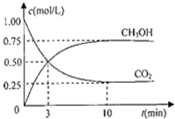 甲醇(CH3OH)是一种优质燃料,
甲醇(CH3OH)是一种优质燃料,查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
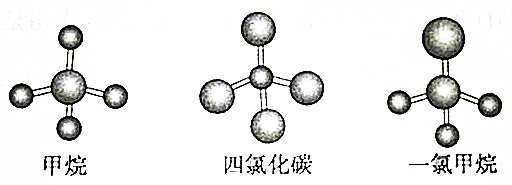
| A. | CH4、CCl4和CH3Cl都是正四面体结构 | |
| B. | CH4、CCl4都是正四面体结构 | |
| C. | CH4和CCl4中的化学键均为非极性键 | |
| D. | CH4、CCl4的结构相同,性质也相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
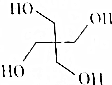 季戊四醇被大量用于涂料工业生产醇酸树脂、合成高级润滑剂、增塑剂、表面活性剂以及医药、炸药等,其结构简式如图所示.季戊四醇可由HCHO与CH3CHO两种有机物按一定比例加成得到的产物与H2再加成得到.则反应中HCHO与CH3CHO的物质的量之比为( )
季戊四醇被大量用于涂料工业生产醇酸树脂、合成高级润滑剂、增塑剂、表面活性剂以及医药、炸药等,其结构简式如图所示.季戊四醇可由HCHO与CH3CHO两种有机物按一定比例加成得到的产物与H2再加成得到.则反应中HCHO与CH3CHO的物质的量之比为( )| A. | 1:1 | B. | 1:2 | C. | 3:1 | D. | 3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
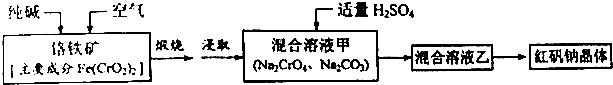
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 正极 | Zn | Cu | Cu | Fe |
| 负极 | Cu | Zn | Zn | Zn |
| 电解质溶液 | CuCl2 | H2SO4 | AgNO3 | CuCl2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com