
【题目】某兴趣小组为了探究铁粉与水蒸气反应的产物,做了下面实验。
资料:在不同温度下,铁粉与水蒸气反应的产物不同。
Fe +H2O![]() FeO+H2 3Fe + 4H2O
FeO+H2 3Fe + 4H2O![]() Fe3O4 + 4H2
Fe3O4 + 4H2
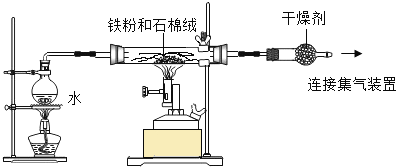
实验一:某兴趣小组用下图所示装置,使铁粉与过量水蒸气充分反应并检验固体产物的组成。
(1)实验过程中,应先点燃___________(选填“酒精灯”或“酒精喷灯”);目的是__________________,装置中石棉绒的作用是_____________________。
(2)若在实验中的某段时间内生成H2 0.2g,则这段时间内参加反应的铁粉质量至少是___________g。
实验二:铁粉完全反应后,兴趣小组对硬质玻璃管中生成的FeO和Fe3O4的质量进行测定,实验流程如下图。
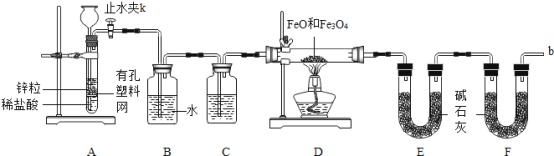
(1)实验前检查装置A的气密性:关闭止水夹K,从长颈漏斗向试管内加水,至长颈漏斗中管内的液面高于管外液面,静置一段时间,若液面高度差__________,则气密性良好。
(2)装置A中发生的反应方程式_______________________________________。
(3)为了安全,在点燃酒精灯之前,在F装置出口b处必须______________________。
(4)装置C中所放试剂为_________,装置B的作用是_________________________。
(5)干燥管E右边又连接干燥管F的目的是_________________________________。
若无干燥管F,测得Fe3O4的质量将_______________(填“偏大”、“偏小”或“无影响”)。
【答案】酒精灯 先产生水蒸气,排尽空气 增大铁粉与水蒸气接触面积 4.2 不变 Zn+2HCl=ZnCl2+H2↑ 验纯 浓硫酸 除去HCl气体 防止空气中的二氧化碳和水蒸气进去到E装置 偏大
【解析】
实验一:(1)铁能与空气中的氧气发生反应,先加热酒精灯利用生成的水蒸气排除装置中的空气;装置中石棉绒可以增大水蒸气与铁粉的接触面积;
(2)分析两个反应可知产生四氧化三铁需要的铁少,因此可依据3Fe+4H2O(g)![]() Fe3O4+4H2,由氢气的质量求出需要铁的质量;
Fe3O4+4H2,由氢气的质量求出需要铁的质量;
实验二:(1)根据检验气密性的方法进行分析解答;
(2)根据锌和盐酸反应产生氯化锌和氢气写出反应方程式;
(3)根据氢气点燃容易发生爆炸分析使用注意事项;
(4)根据产生的氢气会混有杂质,要进行除杂、干燥分析装置的作用;
(5)根据碱石灰会吸收空气中的二氧化碳和水蒸气导致E装置质量增加大,会影响实验结果进行分析。
实验一:
(1)铁能与空气中的氧气发生反应,因此为了排除氧气的干扰,先加热酒精灯利用生成的水蒸气排除装置中的空气;装置中石棉绒可以增大水蒸气与铁粉的接触面积,故答案为:酒精灯;先产生水蒸气,排尽空气;增大铁粉与水蒸气的接触面积;
(2)在不同温度下发生的反应中,Fe元素化合价均升高,H元素化合价均降低,生成一定量H2时,Fe元素化合价升高越高,则所需Fe的量越少,因此根据生成Fe3O4进行计算最少所需Fe的量,设生成0.2g氢气至少需要铁的质量为x,
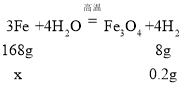 ,则
,则![]() ,解得x=4.2g;
,解得x=4.2g;
实验二:
(1)检查A装置气密性的方法:关闭止水夹K,从长颈漏斗向试管内加水,至长颈漏斗中管内的液面高于管外液面,静置一段时间,形成的液柱不下降,即液面高度差不变,则气密性良好;
(2)锌和盐酸反应产生氯化锌和氢气,故反应的方程式为:Zn+2HCl=ZnCl2+H2↑;
(3)因为氢气在不纯的情况下点燃容易发生爆炸,因此在点燃酒精灯之前,在F装置出口b处必须验纯;
(4)产生的氢气会混有氯化氢和水蒸气,因此要先通过水除去氯化氢,再通过浓硫酸除去水蒸气;故答案为:浓硫酸;除去HCl气体;
(5)碱石灰会吸收空气中的二氧化碳和水蒸气导致E装置质量增加大,会使测定生成的水多,使测定的结果偏大;故答案为:防止空气中的二氧化碳和水被E吸收;偏大。


科目:高中化学 来源: 题型:
【题目】氯化亚铜为白色粉末状固体,难溶于水和乙醇,潮湿时易被氧化,可用作催化剂、杀菌剂、媒染剂等。工业以硫化铜精矿为原料,制备氯化亚铜的流程如图:
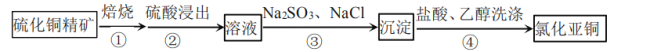
下列说法正确的是( )
A.步骤①焙烧产生的有毒气体可用碱液吸收
B.步骤②所用硫酸浓度越大浸出速率越快
C.步骤③离子方程式:![]()
D.步骤④用乙醇洗涤的目的是使![]() 尽快干燥,防止被空气氧化
尽快干燥,防止被空气氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列叙述正确的是( )
A. 标准状况下,22.4L H2O含有的分子数为1 NA
B. 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA
C. 常温常压下,1 NA 个CO2分子占有的体积为22.4L
D. 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为1 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,只改变反应物中n(SO2)对反应2SO2(g)+O2(g)2SO3(g)的影响如图所示,下列说法正确的是( )
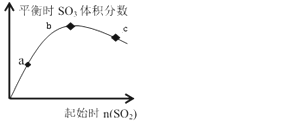
A. 反应a、b、c点均为平衡点,且b点时SO2的转化率最高
B. b点时SO2与O2 的物质的之比约为2:1
C. a、b、c 三点平衡常数: Kb>Kc>Ka
D. a、b、c 三点反应速率大小为: vb>vc>va
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃A与等物质的量的H2O反应生成B,B的一种同系物的溶液可以浸制标本。M是有香味、不易溶于水的油状液体。有关物质的转化关系如下:
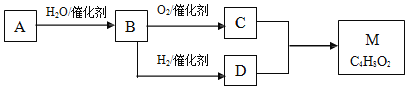
请回答:
(1)写出A的结构简式:______
(2)写出C的官能团的名:______
(3)写出M与NaOH溶液在加热条件下反应的化学反应方程式:______
(4)下列说法不正确的是______
A.烃A在一定条件下可与氯化氢发生反应,再通过加聚反应可得到聚氯乙烯
B.有机物C的溶液可以除去水垢
C.有机物B能与银氨溶液在酒精灯加热的条件下反应产生光亮的银镜
D.有机物C和D发生加成反应生成M
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,组成一个原电池。
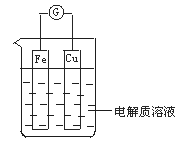
(1)当电解质溶液为稀硫酸时:
①Fe电极是__(填“正”或“负”)极,其电极反应为___。
②Cu电极是__极,其电极反应为___。
(2)由铜、锌和稀硫酸组成的原电池中,铜是__极,电极反应式是__;锌是__极,电极反应式是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在粗食盐中除泥沙外,还含Na2SO4、MgCl2、CaCl2等杂质,工业制精盐除杂时,常常加入过量的除杂剂,现提供下列试剂:a.NaOH溶液;b.盐酸;c.BaCl2溶液;d.Na2CO3溶液,则加入试剂和操作不正确的是( )
A.粗盐![]() 粗盐水
粗盐水![]()
![]()
![]() 滤液
滤液![]() 精盐
精盐
B.粗盐![]() 粗盐水
粗盐水![]()
![]()
![]() 滤液
滤液![]() 精盐
精盐
C.粗盐![]() 粗盐水
粗盐水![]()
![]()
![]() 滤液
滤液![]() 精盐
精盐
D.粗盐![]() 粗盐水
粗盐水![]()
![]()
![]() 滤液
滤液![]() 精盐
精盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO和H2是工业上最常用的合成气,该合成气的制备方法很多,它们也能合成许多重要的有机物。回答下列问题:
(1)制备该合成气的一种方法是以CH4和H2O为原料,有关反应的能量变化如图所示。
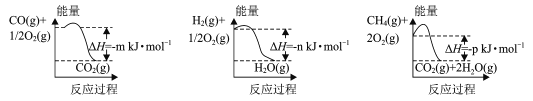
CH4 (g)与H2O(g)反应生成CO(g)和H2 (g)的热化学方程式为____。
(2)工业乙醇也可用CO和H2合成,常含一定量甲醇,各国严禁使用成本低廉的工业酒精勾兑食用酒,但一般定性的方法很难检测出食用酒中的甲醇。有人就用硫酸酸化的橙色K2Cr2O7溶液定量测定混合物中甲醇的含量,甲醇与酸性K2Cr2O7溶液反应生成CO2、Cr2(SO4)3等物质,写出其化学方程式 ___________。
(3)为了检验由CO和H2合成气合成的某有机物M的组成,进行了如下测定:将1.84gM在氧气中充分燃烧,将生成的气体混合物通过足量的碱石灰,碱石灰 增重4. 08 g,又知生成CO2和H2O的物质的量之比为3:4。则M中碳、氢、氧原子个数之比为____。
(4) CO2和H2合成甲醇涉及以下反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g) H=-49.58kJ/mol。在反应过程中可以在恒压的密闭容器中,充入一定量的CO2和H2,测得不同温度下,体系中CO2的平衡转化率与压强的关系曲线如图所示:
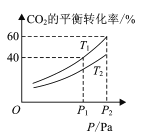
①反应过程中,表明反应达到平衡状态的标志是______;
A.生成3mol O-H键,同时断裂3mol H-H键 B.容器中气体的压强不再变化
C.容器中气体的平均摩尔质量不变 D.CH3OH的浓度不再改变
②比较T1与T2的大小关系:T1 ___T2 (填“<”、“=”或“>”)。
③在T1和P2的条件下,向密闭容器中充入1mol CO2和3mol H2,该反应在第5 min时达到平衡,此时容器的容积为2.4 L,则该反应在此温度下的平衡常数为____,保持T1和此时容器的容积不变,再充入1mol CO2和3mol H2,设达到平衡时CO2的总转化率为a,写出一个能够解出a的方程或式子 ___(不必化简,可以不带单位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由A、B、C、D四种金属按下表中装置进行实验。
装置 |
|
|
|
现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是______________________________________。
(2)装置乙中正极的电极反应式是_______________________________________。
(3)装置丙中溶液的pH________(填“变大”、“变小”或“不变”)。
(4)四种金属活动性由强到弱的顺序是___________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com