
| ʱ��/min | 1 | 2 | 3 | 4 | 5 |
| �������/mL | 50 | 120 | 232 | 290 | 310 |
���� ��1�����ݻ�ѧƽ������ʽ��ʽ���㣬�����2s�ڣ�v��A��Ϊ0.6mol/��L•s��������2sʱ������A���ʵ���=0.6mol/��L•s����SL��2s=1.2Smol
3A��g��+B��g��?2C��g��
��ʼ����mol�� 10 S 0
�仯����mol�� 1.2S 0.4S 0.8S
2s����mol�� 10-1.2S 0.6S 0.8S
���C=$\frac{n}{V}$����B�����ʵ���Ũ�ȣ���ͬ�����£����֮�ȵ������ʵ���֮�ȣ�C ���������=$\frac{C�����ʵ���}{�ܵ����ʵ���}$��100%��
��2���ٸ���Ӱ�컯ѧ��Ӧ���ʵ�������Ũ�ȡ��¶��Լ�����ı������С�����أ��¶�Խ�ߡ�Ũ��Խ��������Խ��Ӧ������Խ�ӱ������ݿ���2 min��3 min�ռ�������������ʱ��ζ࣬ԭ����Zn�û�H2�ķ�Ӧ�Ƿ��ȷ�Ӧ���¶����ߣ�4 min��5 min�ռ���������������Ϊ�淴Ӧ����c��H+���½���
�ڸ���v=$\frac{��C}{��t}$���㷴Ӧ���ʣ�
�۸���Ӱ�컯ѧ��Ӧ���ʵ������Լ���������ȡ����H+�����ʵ����������
��� �⣺��1�����ݻ�ѧƽ������ʽ��ʽ���㣬�����2s�ڣ�v��A��Ϊ0.6mol/��L•s��������2sʱ������A���ʵ���=0.6mol/��L•s����SL��2s=1.2Smol
3A��g��+B��g��?2C��g��
��ʼ����mol�� 10 S 0
�仯����mol�� 1.2S 0.4S 0.8S
2s����mol�� 10-1.2S 0.6S 0.8S
B�����ʵ���Ũ��C��B��=$\frac{n}{V}$=$\frac{0.6S}{S}$mol/L=0.6mol/L
��ͬ�����£����֮�ȵ������ʵ���֮�ȣ�C ���������=$\frac{C�����ʵ���}{�ܵ����ʵ���}$��100%=$\frac{0.8S}{10-1.2S-0.6S+0.8S}$��100%=$\frac{0.8S}{10-S}$��100%��
�ʴ�Ϊ��0.6mol/L��$\frac{0.8S}{10-S}$��100%��
��2����0��1 min��1��2 min��2��3 min��3��4 min��4��5min����ʱ��ε���������ֱ�Ϊ��50 mL��70mL��112 mL��58 mL��20 mL���ӱ������ݿ���2 min��3 min�ռ�������������ʱ��ζ࣬��Ȼ��Ӧ��c��H+���½�������Ҫԭ����Zn�û�H2�ķ�Ӧ�Ƿ��ȷ�Ӧ���¶����ߣ�4 min��5 min�ռ���������������Ȼ��Ӧ�з��ȣ�����Ҫԭ����c��H+���½�����Ӧ��Ũ��Խ�ͣ���Ӧ����ԽС��
�ʴ�Ϊ��4��5min����Ϊ4��5minʱH+Ũ��С�������Ũ��С����
����2��3minʱ����ڣ��������112 mL��n��H2��=$\frac{0.112L}{22.4L/mol}$=0.005mol����2HCl��H2�ã�������������ʵ���Ϊ0.01mol��
��ԣ�HCl��=$\frac{\frac{0.01mol}{0.1L}}{1min}$=0.1 mol/��L•min����
�ʴ�Ϊ��0.1mol/��L•min����
��A����������ˮ����Һ��Ũ�ȼ�С����Ӧ���ʼ�С��H+�����ʵ������䣬��������Ҳ���䣬��A��ȷ��
B�������Ȼ�����Һ����С�����Ũ�ȣ���Ӧ���ʼ�С��H+�����ʵ������䣬��������Ҳ���䣬��B��ȷ��
C������0.5mol/L���ᣬŨ��С��1.0mol/L���ᣬ�൱��ϡ�ͣ���Ӧ���ʼ�С�����������ӣ��������������������ٲ���������������C��ȷ��
��ѡ��ABC��
���� ������Ҫ���鷴Ӧ���ʵļ��㡢��ѧ��Ӧ���ʵ�Ӱ������̽������Ŀ�Ѷ��еȣ���Ҫע����Ƿ�Ӧ������Ũ���Լ��¶ȵı仯�����������˷�����������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��HF��HCl HBr��HI�����Ե�������ʵ���Ƴ�F��Cl��Br��I�ķǽ����Ե����Ĺ��� | |
| B�� | Na��������ȼ����Ҫ����Na2O | |
| C�� | �������ڷǽ���Ԫ�غ���������Դ��������μ��� | |
| D�� | Ԫ����������Ԫ��ԭ�Ӻ�������Ų������Ա仯�Ľ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | a+m+n | B�� | a+m-n | C�� | a-m+n | D�� | a-m-n |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ֳ����м������������⣬�Ƕ����ЧӦЧӦ��ɵ� | |
| B�� | ����β����Ⱦ���к��е�������������Ͳ���ȫȼ����ɵ� | |
| C�� | ����11�ŷɴ�����̫���ܵ�ذ�ɽ�����ת��Ϊ���ܣ�����ת�������Ƕ������� | |
| D�� | ����ʹ�ú�12C�IJ�Ʒ������ʹ�ú�13C��14C�IJ�Ʒ���ϡ��ٽ���̼���á���ּ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ڢۢ� | C�� | �ڢܢ� | D�� | �٢ڢۢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Ľṹʽ��H-Cl-O | B�� | 1H��2H��3H��ͬһ�ֺ��� | ||
| C�� | S2-�Ľṹʾ��ͼ��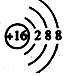 | D�� | ���Ȼ�̼�ĵ���ʽ��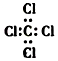 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| �ζ����� | ����Һ����� | |
| �ζ�ǰ�̶�/mL | �ζ���̶�/mL | |
| 1 | 1.04 | 25.03 |
| 2 | 1.98 | 25.99 |
| 3 | 3.20 | 25.24 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������ۼ�����Ϊ0.4NA�İ��ף�P4���ͼ�������ʵ������ | |
| B�� | 10gŨ��Ϊ46%���Ҵ�ˮ��Һ�к��е���ԭ������Ϊ1.2NA | |
| C�� | 2 g H2�ֱ���������C12��N2��ַ�Ӧ��ת�Ƶĵ�������Ϊ2NA | |
| D�� | 1molFe��OH��3�뺬3molHI����Һ��ȫ��Ӧ����Һ������I-����ĿΪ3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶�/�� | 1 000 | 1 150 | 1 300 |
| ƽ�ⳣ�� | 4.0 | 3.7 | 3.5 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com