



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ˮ����������ױ��������� |
| B�������Ը��������Һ�����ұ�������ϩ�ͻ����� |
| C����̼������Һ�����Ҵ���������������� |
| D����ȼ�շ�����״����������Ȼ�̼ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Ԫ�ش��� | L | M | Q | R | T |
| ԭ�Ӱ뾶/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| ��Ҫ���ϼ� | +2 | +3 | +6��-2 | +2 | -2 |
| A��R���������Ӧ��ˮ������ܾ������� |
| B��L��Q�γɵļ����Ӻ����������� |
| C��T��Q���⻯�ﳣ̬�¾�Ϊ��ɫ���� |
| D��L��M�ĵ�����ϡ���ᷴӦ���ʣ�M��L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
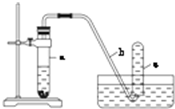 ����ͼ��ʾ��װ�ý���ʵ�飺
����ͼ��ʾ��װ�ý���ʵ�飺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
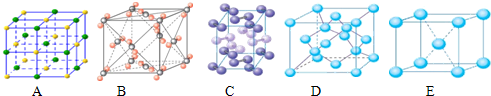
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� |
| ���� |
| ʵ����� | �¶ȡ� | ��ʼCCl4Ũ�ȣ�mol?L-1�� | ��ʼH2Ũ�ȣ�mol?L-1�� | CCl4��ת���� |
| 1 | 110 | 0.8 | 1.2 | A |
| 2 | 110 | 1 | 1 | 50% |
| 3 | 100 | 1 | 1 | B |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CO��CO2���Ԫ����ͬ�����ܽ�Fe2O3��ԭ��Fe |
| B��SiO2��CO2��Ϊ���������������NaOH��Һ��Ӧ������ |
| C��Na2O��Na2O2Ϊ��ͬԪ����ɵĽ���������� CO2��Ӧ������ͬ |
| D��Ũ���ᡢŨ���ᡢϡ���������ǿ�����ԣ������¾�������������ʢ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com