
| Ԫ�� | H | Li | Be | B | C | N | O | F |
| �縺�� | 2.1 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 | 4.0 |
| Ԫ�� | Na | Mg | Al | Si | P | S | Cl | K |
| �縺�� | 0.9 | 1.2 | 1.5 | 1.7 | 2.1 | 2.3 | 3.0 | 0.8 |
���� ��1���縺�Ա�ʾ�Լ��ϵ��ӵ����������縺��Խ��Լ��ϵ���������Խ�����Էǽ�����Խǿ�縺��Խǿ���ʵ縺����ǿ�����������ڱ������Ͻǣ�����Ԫ�س��⣩��
�ɱ������ݿ�֪��ͬ����������ҵ縺������ͬ�������϶��µ縺�Խ��ͣ�
��2���ɱ������ݿ�֪��ͬ����������ҵ縺������ͬ�������϶��µ縺�Խ��ͣ��ʷǽ�����Խǿ�縺��Խ������Խǿ�縺��ԽС��
��3��AlCl3�����縺��֮��Ϊ1.5��BrԪ�صĵ縺��С��ClԪ�ص縺�ԣ�AlBr3�����縺��֮��С��1.5��
��� �⣺��1���縺�Ա�ʾ�Լ��ϵ��ӵ����������縺��Խ��Լ��ϵ���������Խ�����Էǽ�����Խǿ�縺��Խǿ���ʵ縺����ǿ�����������ڱ������Ͻ�ΪFԪ�أ�
�ɱ������ݿ�֪��ͬ����������ҵ縺������ͬ�������϶��µ縺�Խ��ͣ��ʸ�Ԫ�صĵ縺�Ա�KԪ�ش�С��MgԪ�صĵ縺�ԣ���0.8��X��Ca����1.2��
�ʴ�Ϊ��F��0.8��1.2��
��2���ɱ������ݿ�֪��ͬ����������ҵ縺������ͬ�������϶��µ縺�Խ��ͣ��ʷǽ�����Խǿ�縺��Խ������Խǿ�縺��ԽС��
�ʴ�Ϊ�����϶��µ縺�Խ��ͣ��ǽ�����Խǿ�縺��Խ������Խǿ�縺��ԽС��
��3��AlCl3�����縺��֮��Ϊ1.5��BrԪ�صĵ縺��С��ClԪ�ص縺�ԣ�AlBr3�����縺��֮��С��1.5����AlBr3�л�ѧ��Ϊ���ۼ���
�ʴ�Ϊ�����ۼ���AlCl3�����縺��֮��Ϊ1.5��BrԪ�صĵ縺��С��ClԪ�ص縺�ԣ�AlBr3�����縺��֮��С��1.5��
���� ���⿼��ԭ�ӽṹ��Ԫ�������ʣ��漰�縺�Լ�������Էǽ����ԵĹ�ϵ�ȣ�Ϊ��Ƶ���㣬�Ѷ��еȣ��������Ԫ�ص縺�Եĵݱ�����ǽ���ؼ���


 Сѧ������ҵϵ�д�
Сѧ������ҵϵ�д� ��ʿһ��ȫͨϵ�д�
��ʿһ��ȫͨϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
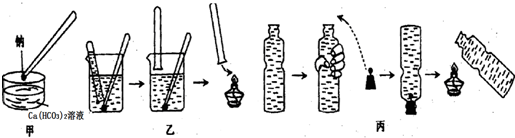
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
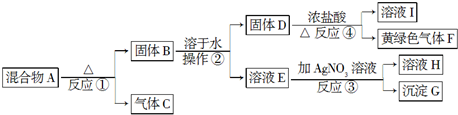


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ȼ�����Һ�����������յò����Ȼ������� | |
| B�� | ���ȵĴ�����Һ��ϴ����Ч���� | |
| C�� | ��H2��I2��HI��ɵ�ƽ����ϵ��ѹ���������ɫ���� | |
| D�� | �����£���1 mL pH=3�Ĵ�����Һ��ˮϡ����100 mL�������pH��5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
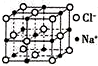 ��C��N��O��Na��Fe����Ԫ����ɵ������Na2[Fe��CN��5��NO��]���������Ƹ�Ѫѹ��֢��
��C��N��O��Na��Fe����Ԫ����ɵ������Na2[Fe��CN��5��NO��]���������Ƹ�Ѫѹ��֢�� ��δ�ɶԵ�����Ϊ5��
��δ�ɶԵ�����Ϊ5���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��BaSO4����ˮ�в��ܵ��磬�������ᱵ���ǵ���� | |
| B�� | NaCl��Һ�ܵ��磬����NaCl��Һ�ǵ���� | |
| C�� | �Ȼ�������ˮ�ܵ��磬��Һ̬�Ȼ��ⲻ�ܵ��� | |
| D�� | ��̬��NaCl�����磬����̬NaCl���Ե��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����CO2ͨ����Һ�У�2NaCN+H2O+CO2=2HCN+Na2CO3 | |
| B�� | ���ⶨCH3COONH4��ˮ��Һ�����Կ�֪��K��NH3•H2O��=1.75��10-5 | |
| C�� | �������ʵ���Ũ�ȵ�CH3COONa��NaCN��Һ�������Ϻ����Һ�У�c��CH3COO-����c��CN-�� | |
| D�� | �����½�10ml��PH=3�Ĵ�����Һϡ�͵�100ml����PH��4 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com