
 ��
�� ��
�� ��
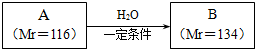
������ ��A������C��H��O����Ԫ�ص�������Ϊ12��1��16��A������C��H��O����Ԫ�ص�ԭ�Ӹ�����Ϊ$\frac{12}{12}$��$\frac{1}{1}$��$\frac{16}{16}$=1��1��1��ʵ�����A��ʹ��ˮ��ɫ��1mol A ������NaHCO3 ��Һ��Ӧ�ų�2molCO2����A�к���-C=C-��2��-COOH��A����Է�������Ϊ116��116-90-24=2��������к���2��Hԭ�ӣ���AΪHOOC-CH=CH-COOH��HOOC-C��COOH��=CH2��A�������ᷴӦֻ�ܵõ�һ�ֲ������Aֻ��ΪHOOC-CH=CH-COOH��B����Է�������Ϊ134��134-116=18����A��B����̼̼˫����ˮ�ļӳɷ�Ӧ������B�к���-OH��-COOH����BΪHOOC-CH2CH��OH��-COOH��Ȼ�������ʵĽṹ�����������
��� �⣺��1��A�к�̼̼˫�����Ȼ���BΪHOOC-CH2CH��OH��-COOH�������ʽΪC4H6O5���ʴ�Ϊ��̼̼˫�����Ȼ���C4H6O5��
��2��A�������ᷴӦֻ�ܵõ�һ�ֲ������Aֻ��ΪHOOC-CH=CH-COOH���ʴ�Ϊ��HOOCCH=CHCOOH��
��3��B������Ҵ���Ӧ�Ļ�ѧ����ʽΪ ��
��
�ʴ�Ϊ�� ��
��
��4��B ʧȥ1 ����ˮ�����γ�һ����Ԫ��״������C����C�Ľṹ��ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��5��B�к���-OH��-COOH��BΪHOOC-CH2CH��OH��-COOH���京��ͬ�����ŵ�B ��ͬ���칹��ṹ��ʽΪ ��
��
�ʴ�Ϊ�� ��������һ�֣���
��������һ�֣���
��6��BΪHOOC-CH2CH��OH��-COOH��-OH��-COOH����Na��Ӧ��ֻ��-COOH��NaOH��NaHCO3��Ӧ����1molB����Na��NaOH��Һ��NaHCO3��Һ��ַ�Ӧ������Na��NaOH��NaHCO3���ʵ���֮��Ϊ3��2��2���ʴ�Ϊ��3��2��2��
���� ���⿼���л�����ƶϣ�Ϊ��Ƶ���㣬��ȷA��B�Ľṹ��A�����ʡ�A��B�����ӳ��ǽ�����ͻ�ƿڣ���ϣ�2��ȷ��A�Ľṹ�ǽ����Ĺؼ����ط������ƶ��������л���ṹ�����ʵĿ��飬��Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ѧ�Ҹ����ڹ��˴�����Ϣ������ȡ��ͻ���Գɾͣ����˵���Ҫ�ɷ��Ǹߴ��ȵĶ������� | |
| B�� | ��ҵ����ʯ�Ҷ�úȼ�պ��γɵ��������������ܻ��յõ�ʯ�� | |
| C�� | ���������������ȼú����������β����������������߿������� | |
| D�� | ���MgCl2��Һ�����Ƶý���þ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ����ɷ� | ����ɷ� | |
| A | Na2CO3 | CO2��H2O��O2 |
| B | Na2CO3 | H2O��O2 |
| C | Na2CO3��Na2O2 | O2 |
| D | Na2CO3��Na2O2��NaOH | O2 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����������������£�����������Ӧ | |
| B�� | ����Һ���Ϻ�������� | |
| C�� | ��ϩͨ����ˮ�� | |
| D�� | �������ȵ�ͭ˿�����Ҵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com