
(本小题15分) A、B、C、D四种元素原子核电荷数依次增大(均小于20),其单质及相应的化合物能发生如下反应关系:
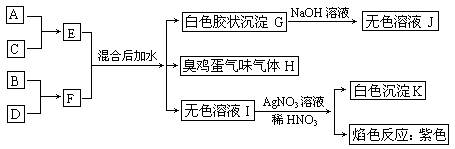
(1)写出四种元素元素符号:A、____B、____C、____D、____。
(2) F的电子式:_________________。
(3)写出E、F混合后加水的化学方程式:_________________________________。
(4)写出GJ的化学方程式:_________________________________。
(5)写出C单质与H水溶液反应的离子方程式:_____________________________。
(1) Al S Cl K(4分)
(2) ![]() (2分)
(2分)
(3) 2AlCl3+3K2S+3H2O=2Al(OH)3↓+3H2S↑+6KCl(3分)
(4) Al(OH)3+NaOH=NaAlO2+2H2O(3分)
(5) Cl2+H2S=S↓+2H++2Cl- (3分)
考查盐类的双水解,两性氢氧化物,卤离子的检验,焰色反应等知识以及综合应用能力、分析判断与逻辑推理能力,同时考查学生的化学用语等。框图中有几个特征的反应现象:a 臭鸡蛋气味气体;b 白色胶状沉淀溶于NaOH溶液;c 先加AgNO3溶液,再加稀HNO3产生白色沉淀;d 焰色反应:紫色;可分别得出气体是H2S、白色胶状沉淀是Al(OH)3、无色溶液I是KCl。技能空间:常见的特征反应现象及对应物质:
⑴焰色反应:Na黄色,K紫色(透过钴玻璃)。
⑵有臭鸡蛋气味或能使湿润的Pb(Ac)2试纸变黑的气体是H2S。
⑶在空气中由无色迅速变为红棕色的气体是NO。
⑷使品红溶液褪色的往往是SO2 (Cl2使品红溶液褪色后不恢复) 。
⑸能使淀粉变蓝的是I2。
⑹与碱溶液反应生成白色沉淀且放置空气中变灰绿色最终变红褐色的离子是Fe2+。
⑺滴入SCN- 溶液显血红色以及遇苯酚显紫色的离子是Fe3+。
⑻既能跟酸反应又能跟碱反应且生成气体的物质一般是Al,NH4HCO3 ,(NH4)2CO3 ,NH4HSO3,(NH4)2SO3,(NH4)2S,NH4HS。
⑼能使湿润的红色石蕊试纸变蓝的气体是NH3。
⑽与碱反应产生气体的物质是Al、Si、铵盐,产生气体一般是H2、NH3。
⑾与水反应产生气体的物质一般是Na 、F2 、Na2O2。
⑿既能与酸反应又能与碱反应的物质是Al 、Al2O3、Al(OH)3、弱酸弱碱盐、弱酸的酸式盐。
⒀既产生沉淀又产生气体的物质一般是CaC2、Al2S3、Mg3N2 与H2O; S2O32-与H+;CO32-、HCO3-、 SO32-、 HSO3-、 S2-、HS- 与Al3+;CO32-、HCO3-与Fe3+。
应试策略:有些框图推断题,从题干看,基本得不出什么直接的结论。框图中的特征反应及现象往往是解决问题的突破口即题眼。解题时可从上述特征反应及现象直按入手,结合框图中提供的转化关系,往往能迅速得出其他结论。


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案科目:高中化学 来源: 题型:
(本小题15分)为测定空气中CO2含量,做下述实验。
| 配0.1mol/L的标准盐酸和0.01mol/L的标准盐酸 | → | 用0.1mol/L的标准盐酸滴定未知Ba(OH)2溶液10mL用去盐酸19.60 mL | → | 用Ba(OH)2溶液吸收空气中的CO2 | → | 过 滤 | → | 取滤液20mL,用0.01mol/L的盐酸滴定用去盐酸34.8mL |
(1)为配置标准溶液,请选取必需的一组仪器 。
①托盘天平 ②容量瓶 ③滴定管 ④量筒 ⑤烧杯 ⑥胶头滴管 ⑦玻璃棒
A.①②⑤⑥ B.②④⑤⑥⑦ C.②①⑥⑦ D.②④⑤⑥
(2)滴定操作时,左手 ,眼睛注视 。
(3)取上述Ba(OH)2溶液10mL放入100mL容量瓶中,加水稀释至刻度,把稀释后的溶液放入密闭容器,并引入10L空气,振荡,过滤。需过滤的原因是 。
(4)由实验数据算出空气中CO2的体积分数为 。
(5)本实验中,若第一次滴定时使用的酸式滴定管未经处理,即更换溶液,进行第二次滴定,导致实验数据值(填偏高、偏低或无影响) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(本小题15分) A、B、C、D四元素的核电荷数依次增加,它们的离子的电子层数相同且最外层电子数均为8。A原子的L层电子数与K、M层电子数之和相等,D原子的K、L层电子数之和等于电子总数的一半。回答以下问题:
(1)四元素的符号依次是A______;B______;C________;D______。
(2)写出B、D元素的离子结构示意图:
B.______________________; D.______________________。
(3)用电子式表示A、C元素形成的离子化合物的过程:
________________________________________________________。
(4)在A、B、C、D最高价氧化物水化物中:
比较其中酸的酸性强弱:____________________________;
比较其中碱的碱性强弱:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(本小题15分)用二氧化氯(ClO2)、铁酸钠(Na2FeO4摩尔质量为166 g·mol-1)等新型净水剂替代传统的净水剂Cl2对淡水进行消毒是城市饮用水处理新技术。ClO2和Na2FeO4在水处理过程中分别被还原为Cl-和Fe3+。
(1)如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么,ClO2、Na2FeO4、Cl2三种消毒杀菌剂的消毒效率由大到小的顺序是 > > 。
(2)铁酸钠之所以能净水,除它本身具有强氧化性外,另一个原因可能是:
。

(3)二氧化氯是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。ClO2可以看做是亚氯酸(HClO2)和氯酸(HClO3)的混合酸酐。工业上用稍潮湿的KClO3和草酸在60℃时反应制得。某学生用如图所示的装置模拟工业制取及收集ClO2,其中A为ClO2的发生装置,B为ClO2的凝集装置,C为尾气吸收装置。请问:
①A部分还应添加温度控制(如水浴加热)装置,B部分还应补充什么装置 ;
②C中应装的试剂为 。C中发生反应的化学方程式为:
。
查看答案和解析>>
科目:高中化学 来源: 题型:
(本小题15分)已知一定条件下丙烯的浓HBr能发生如下反应:
CH3-CH=CH2 + H-Br CH3--CH3
化合物A和A’互为同分异构体,元素分析含溴58.4%(其它元素数据不全,下同)。A和A’有如下系列反应,其中气态物质B是烃,含碳85.7%;C’不发生类似图中C的系列转化;E为酸性物质,其中碳氢含量共为63.6%。
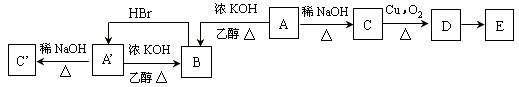
请回答下列问题:
(1)写出结构简式:A ,B: 。
(2)写出下列转化关系的化学方程式:
①B→A’ : 。
②C→D: 。
③D→E: 。
(3)简述检验A中含有溴元素的实验方法:
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com