
分析 (1)根据n=$\frac{m}{M}$计算二氧化碳物质的量,再根据m=nM计算其质量,根据N=nNA计算分子数目,含有原子数目为二氧化碳分子的3倍;
(2)根据n=$\frac{m}{M}$判断物质的量关系,物质的量越大含有分子数目越多,同温同压下气体的体积越大.
解答 解:(1)标况下5.6L的CO2物质的量为$\frac{5.6L}{22.4L/mol}$=0.25mol,其质量为0.25mol×44g/mol=11g,含有分子数目为0.25mol×NAmol-1=0.25NA,含有原子数目为0.25NA×3=0.75NA,
故答案为:11;0.25NA;0.75NA;
(2)由于 M(CO2)>M(HCl)>M(O2)>M(NH3),根据n=$\frac{m}{M}$可知,n(CO2)<n(HCl)<n(O2)<n(NH3),物质的量越大含有分子数目越多,同温同压下气体的体积越大,故所含分子数目最少的是CO2,体积最大的是NH3,
故答案为:CO2;NH3.
点评 本题考查物质的量有关计算,比较基础,注意掌握以物质的量为中心的计算.


 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案科目:高中化学 来源: 题型:多选题

| A. | 反应方程式中n=2 | |
| B. | 该反应的△S>0 | |
| C. | 10 min时,曲线发生变化的原因是增大压强 | |
| D. | 0~5min内,平均反应速率v(X)=0.04 mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L H2O含有的分子数为NA | |
| B. | 2.7g铝与足量氢氧化钠溶液反应转移的电子数NA | |
| C. | 0.5 mol/L Fe2(SO4)3溶液中,SO42-的数目为1.5NA | |
| D. | 常温常压下,48 g O2和O3 的混合物中含有的氧原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑤④③①⑥ | B. | ④①②⑤③⑥ | C. | ④②①③⑤⑥ | D. | ⑤②④①③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | MOH和ROH都是强碱 | |
| B. | 稀释前,c(ROH)=10c(MOH) | |
| C. | 在x点,c(M+)=c(R+) | |
| D. | 中和等体积未稀释的MOH和ROH溶液,所需HCl的物质的量:ROH>MOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
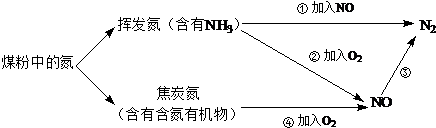
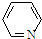 ),其分子中相邻的C和N原子相比,N原子吸引电子能力更强(填“强”或“弱”),从原子结构角度解释原因:C和N在周期表的位置是同一周期从左到右,N 的原子半径更小,原子核对外层电子的吸引力更强.
),其分子中相邻的C和N原子相比,N原子吸引电子能力更强(填“强”或“弱”),从原子结构角度解释原因:C和N在周期表的位置是同一周期从左到右,N 的原子半径更小,原子核对外层电子的吸引力更强.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH溶液保存在带玻璃塞试剂瓶中 | B. | 氯水保存棕色细口瓶中 | ||
| C. | 钠保存在煤油中 | D. | 液氯可以保存在干燥的钢瓶中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com