
| A. | 硫化氢在氧气中燃烧 | B. | 铁在硫蒸气中燃烧 | ||
| C. | 二氧化硫通入石灰水中 | D. | 硫酸中加入铁粉 |
分析 A.反应产物与氧气的量有关;
B.反应只生成FeS;
C.反应产物与二氧化硫的量有关;
D.反应产物与硫酸浓度有关.
解答 解:A.硫化氢在少量氧气中燃烧生成S、水,硫化氢在足量氧气中燃烧生成二氧化硫、水,故A不选;
B.变价金属铁与硫反应,硫的氧化性弱只能生成FeS,与量无关,故B选;
C.二氧化硫通入石灰水,二氧化硫过量则生成亚硫酸氢钙,2SO2+Ca(OH)2═Ca(HSO3)2,氢氧化钙过量则生成亚硫酸钙,Ca(OH)2+SO2═CaSO3↓+H2O,反应物用量不同,产物不同,故C不选;
D.Fe与稀硫酸发生H2SO4+Zn═ZnSO4+H2↑,Fe与浓硫酸发生2Fe+6H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Fe2(SO4)3+3SO2↑+6H2O,硫酸浓度不同,产物不同,故D不选;
故选B.
点评 本题考查物质的性质,为高频考点,侧重元素化合物知识的考查,把握物质的性质、发生的反应为解答的关键,注意与量或浓度有关的反应,题目难度不大.


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:选择题
| A. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl是取代反应 | |
| B. | CH2=CH2+Br2→CH2Br-CH2Br是加成反应 | |
| C. | 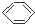 +HO-NO2$→_{60℃}^{浓硫酸}$ +HO-NO2$→_{60℃}^{浓硫酸}$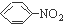 +H2O是取代反应 +H2O是取代反应 | |
| D. | 2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O是加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 铜是阳极,铜片上有气泡产生 | |
| B. | 铜离子在铜片表面被还原 | |
| C. | 电流从锌片经导线流向铜片 | |
| D. | 反应中,盐桥中的K+会移向ZnSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H2+O2 $\frac{\underline{\;点燃\;}}{\;}$2H2O | |
| B. | CaO+H2O=Ca(OH)2 | |
| C. | CaCO3 $\frac{\underline{\;\;△\;\;}}{\;}$CaO+CO2↑ | |
| D. | CH3CH2OH(酒精)+3O2 $\frac{\underline{\;点燃\;}}{\;}$2CO2+3 H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
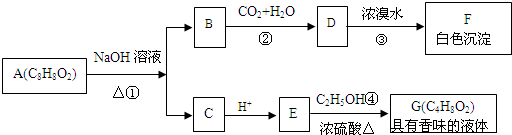
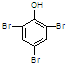 ;
;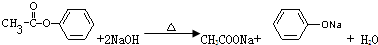 ;
;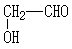 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
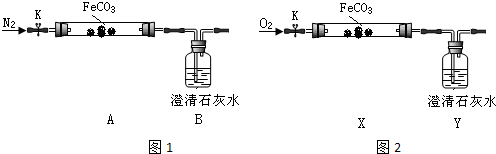
| 实验编号 | 实验步骤 | 实验现象 |
| i | 向甲溶液滴加KSCN溶液 | 溶液变红色 |
| ii | 向乙溶液滴加酸性高锰酸钾溶液 | 溶液不褪色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com