
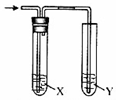
 用图所示装置进行相关实验,能达到实验目的是( )
用图所示装置进行相关实验,能达到实验目的是( )| 实验 | 试剂X | 试剂Y | |
| A | 检验乙醇与浓硫酸共热产生的乙烯 | NaHSO3溶液 | KMnO4酸性溶液 |
| B | 检验CO2和SO2混合气体中的CO2 | 品红溶液 | 澄清的石灰水 |
| C | 除去Cl2中混有的HCl,并验证Cl2的漂白性 | 饱和NaCl溶液 | 品红溶液 |
| D | 通入 HCl,验证非金属性Cl>C>Si | NaHCO3溶液 | Na2 SiO3溶液 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.乙醇易挥发,且可能生成二氧化硫,乙烯、二氧化硫均能使高锰酸钾褪色;
B.品红可检验二氧化硫,但二氧化硫、二氧化碳均使石灰水变浑浊;
C.食盐水可除去HCl,抑制氯气的溶解,氯气与水反应生成HClO可漂白;
D.HCl为无氧酸,发生强酸制取弱酸的反应,但利用最高价含氧酸的酸性比较非金属性.
解答 解:A.乙醇易挥发,且可能生成二氧化硫,乙烯、二氧化硫均能使高锰酸钾褪色,则不能检验乙烯,故A错误;
B.品红可检验二氧化硫,但二氧化硫、二氧化碳均使石灰水变浑浊,没有除去二氧化硫的干扰,不能检验二氧化碳,故B错误;
C.食盐水可除去HCl,抑制氯气的溶解,氯气与水反应生成HClO可漂白,则可实现实验目的,故C正确;
D.HCl为无氧酸,发生强酸制取弱酸的反应,但利用最高价含氧酸的酸性比较非金属性,不能比较非金属性,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握实验装置的作用、物质的性质及反应、物质的检验、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标况下,11.2L 氟化氢中含有的分子数目为0.5NA | |
| B. | 室温下,21.0g乙烯和丁烯的混合气体中所含的碳原子数目是NA | |
| C. | 室温下,2L0.05mol/L 的NH4NO3溶液中所含有的氮原子数目是0.2NA | |
| D. | 22.4L Cl2 与足量NaOH溶液反应时转移的电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | ②③④⑤ | C. | ①③④ | D. | ①②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用氨水吸收过量的二氧化硫:NH3•H2O+SO2═HSO3-+NH4+ | |
| B. | 用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+H2O2+2H+═I2+2H2O | |
| C. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42-完全沉淀:2Ba2++Al3++2SO42-+4OH-═AlO2-+2BaSO4↓+2H2O | |
| D. | 向含0.1mol•L-1Na2CO3和0.2mol•L-1NaOH的混合溶液中加入等体积的0.15mol•L-1的硫酸:CO32-+3H++2OH-═2H2O+HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | -(a+$\frac{b}{2}$+c)kJ/mol | B. | +(a+$\frac{b}{2}$+c)kJ/mol | C. | -(2a+b+2c)kJ/mol | D. | +(2a+b+2c)kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 组号 | 反应温度 /℃ | 参加反应物质 | ||||
| KMnO4 | H2C2O4 | MnSO4 | ||||
| V/mL | c/mol•L-1 | V/mL | c/mol•L-1 | m/g | ||
| A | 20 | 4 | 0.1 | 2 | 0.1 | 0 |
| B | 20 | 4 | 0.1 | 2 | 0.1 | 0.1 |
| C | 40 | 4 | 0.1 | 2 | 0.1 | 0 |
| D | 40 | 4 | 0.1 | 2 | 0.2 | 0.1 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高一上10月月考化学试卷(解析版) 题型:选择题
质量分数为a的某物质的溶液m g与质量分数为b的该物质的溶液n g混合后,蒸发掉p g水。得到的溶液每亳升质量为q g,物质的量浓度为c。则溶质的相对分子质量为( )
A. 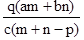 B.
B. 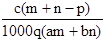 C.
C. 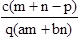 D.
D. 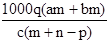
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com