【答案】
分析:A、B、C、D、E是化学中常见的物质,常温下,E是一种无色无味的液体,则E为H
2O,
(1)A是一种黑色单质,B是一种常见的难挥发性酸,C、D都是气体,则A为C,B为浓硫酸,C、D分别为二氧化碳、二氧化硫中的一种;
(2)A是一种紫红色单质,B是一种常见的挥发性酸,反应时生成的C是无色气体,则A为Cu,B为稀硝酸,C为NO,D为硝酸铜;
(3)C是一种无色、刺激性气味、密度比空气小的气体,则C为NH
3,实验室利用铵盐与熟石灰反应制备氨气,利用湿润的红色石蕊试纸检验氨气,以此来解答.
解答:解:A、B、C、D、E是化学中常见的物质,常温下,E是一种无色无味的液体,则E为H
2O,
(1)A是一种黑色单质,B是一种常见的难挥发性酸,C、D都是气体,则A为C,B为浓硫酸,C、D分别为二氧化碳、二氧化硫中的一种,该反应为C+2H
2SO
4(浓)
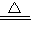
CO
2↑+2H
2O+SO
2↑,故答案为:C+2H
2SO
4(浓)
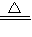
CO
2↑+2H
2O+SO
2↑;
(2)A是一种紫红色单质,B是一种常见的挥发性酸,反应时生成的C是无色气体,则A为Cu,B为稀硝酸,C为NO,D为硝酸铜,反应的离子反应为2NO
3-+3Cu+8H
+=2NO↑+4H
2O+3Cu
2+,生成硝酸铜体现硝酸的酸性,生成NO体现硝酸的氧化性,故答案为:2NO
3-+3Cu+8H
+=2NO↑+4H
2O+3Cu
2+;酸性;氧化性;
(3)C是一种无色、刺激性气味、密度比空气小的气体,则C为NH
3,实验室利用铵盐与熟石灰反应制备氨气,该反应为2NH
4Cl+Ca(OH)
2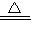
CaCl
2+2NH
3↑+2H
2O;检验方法为把湿润的红色石蕊试纸靠近气体,若试纸变蓝,则证明该气体为氨气(或用蘸有浓盐酸的玻璃棒靠近该气体,若有白烟生成,则证明该气体为氨气),
故答案为:2NH
4Cl+Ca(OH)
2
CaCl
2+2NH
3↑+2H
2O;把湿润的红色石蕊试纸靠近气体,若试纸变蓝,则证明该气体为氨气(或用蘸有浓盐酸的玻璃棒靠近该气体,若有白烟生成,则证明该气体为氨气).
点评:本题考查无机物的推断,侧重物质性质的考查,涉及浓硫酸、浓硝酸的性质及氨气的制备,明确发生的化学反应即可解答,题目难度中等.

 CO2↑+2H2O+SO2↑,故答案为:C+2H2SO4(浓)
CO2↑+2H2O+SO2↑,故答案为:C+2H2SO4(浓) CO2↑+2H2O+SO2↑;
CO2↑+2H2O+SO2↑;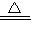 CaCl2+2NH3↑+2H2O;检验方法为把湿润的红色石蕊试纸靠近气体,若试纸变蓝,则证明该气体为氨气(或用蘸有浓盐酸的玻璃棒靠近该气体,若有白烟生成,则证明该气体为氨气),
CaCl2+2NH3↑+2H2O;检验方法为把湿润的红色石蕊试纸靠近气体,若试纸变蓝,则证明该气体为氨气(或用蘸有浓盐酸的玻璃棒靠近该气体,若有白烟生成,则证明该气体为氨气),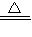 CaCl2+2NH3↑+2H2O;把湿润的红色石蕊试纸靠近气体,若试纸变蓝,则证明该气体为氨气(或用蘸有浓盐酸的玻璃棒靠近该气体,若有白烟生成,则证明该气体为氨气).
CaCl2+2NH3↑+2H2O;把湿润的红色石蕊试纸靠近气体,若试纸变蓝,则证明该气体为氨气(或用蘸有浓盐酸的玻璃棒靠近该气体,若有白烟生成,则证明该气体为氨气).

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案

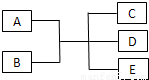
 已知A、B、C、D、E五种物质有如图所示的转化关系(部分反应物及反应条件未列出,若解题时需要,可作合理假设),且五种物质中均含有A元素.
已知A、B、C、D、E五种物质有如图所示的转化关系(部分反应物及反应条件未列出,若解题时需要,可作合理假设),且五种物质中均含有A元素. (Ⅰ)通常情况下,微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀.请回答:
(Ⅰ)通常情况下,微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀.请回答: