
| A. | 改用100mL2mol•L-1盐酸 | B. | 加入碳酸钠固体 | ||
| C. | 滴加少量CuCl2溶液 | D. | 降低温度 |
分析 能加快反应速率且不影响氢气的总量,盐酸的量一定,可以通过升高温度、增大盐酸浓度、加入某些物质形成原电池但改变条件时不能改变氢离子的总物质的量,据此分析解答.
解答 解:A.改用100mL2mol•L-1盐酸,氢离子浓度增大,反应速率加快,但盐酸的物质的量增大,所以生成氢气总量增大,故A错误;
B.加入碳酸钠固体,碳酸钠和稀盐酸反应生成二氧化碳,所以导致生成氢气总量减少,故B错误;
C.加入少量氯化铜,Zn和氯化铜反应生成Cu,Cu、Zn和稀盐酸构成原电池,加快反应速率,且盐酸的总物质的量不变,所以生成氢气总量不变,故C正确;
D.降低温度,减小活化分子百分数,所以反应速率降低,故D错误;
故选C.
点评 本题考查化学反应速率影响因素,为高频考点,明确浓度、温度、反应物接触面积对化学反应速率影响原理是解本题关键,注意题干中限制性条件“增大反应速率、生成氢气总量不变”,题目难度不大.


科目:高中化学 来源: 题型:解答题
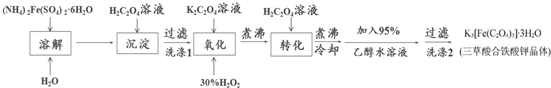
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作 | 实验现象 | 实验结论 | |
| A | 向蛋白质溶液中加入饱和硫酸铵溶液 | 有白色沉淀析出,再加水,沉淀溶解 | 硫酸铵使蛋白质变性 |
| B | 将乙醇与酸性重铬酸钾(K2Cr2O7)溶液混合 | 橙色溶液变为绿色 | 乙醇具有还原性 |
| C | 蔗糖溶液中加入稀硫酸,水解后加入银氨溶液,水浴加热 | 未出现银镜 | 蔗糖的水解产物为非还原性糖 |
| D | 将新制Cu(OH)2与葡萄糖溶液混合加热 | 产生砖红色沉淀(Cu2O) | 葡萄糖具有氧化性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
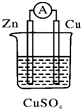
| A. | 电流从锌电极通过电流表流向铜电极 | |
| B. | 锌电极发生还原反应,铜电极发生氧化反应 | |
| C. | 当有13 g Zn溶解时,外电路中就有0.4 mol电子通过 | |
| D. | 铜电极作正极,发生的电极反应为2H++2e-═H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 1 | ① | |||||||
| 2 | ⑤ | ⑥ | ⑦ | |||||
| 3 | ② | ③ | ④ | ⑧ | ||||
| 4 | ⑨ | |||||||
| 5 | ⑩ |
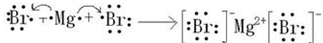 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素的最高正化合价在数值上一定等于它所在的族序数 | |
| B. | 同周期主族元素的原子半径越小,越难得到电子 | |
| C. | 氟气能从溴化钾溶液中置换出溴单质 | |
| D. | 酸性:HClO4>H2SO4>H3PO4>H2SiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
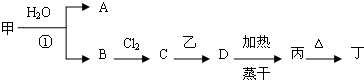
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L 0.1mol/L的NaHS溶液中HS-和S2-离子数之和为0.1NA | |
| B. | 2.0 g H218O与D2O的混合物中所含中子数为NA | |
| C. | 1 mol Na2O2固体中含离子总数为4NA | |
| D. | 3 mol Fe在足量的水蒸气中完全反应转移9NA个电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com