
A.5”Ć2 B.2”Ć5? C.2”Ć1 D.1”Ć1?
½āĪö£ŗ“æ¼īÓėŃĪĖį·“Ó¦Ź±£¬²Ł×÷Ė³Šņ²»Ķ¬·“Ó¦½ų³ĢŅ²²»Ķ¬”£?
²Ł×÷¢Ł£ŗ“æ¼īµĪČėŃĪĖįÖŠ£¬·¢Éś·“Ó¦£ŗ?
Na2CO3+2HCl![]() 2NaCl+CO2ӟ+H2O
2NaCl+CO2ӟ+H2O
Éś³ÉµÄCO2ÓėŃĪĖįÓĆĮæÓŠ¹Ų£ŗ?
n(CO2)=![]() n (HCl)=
n (HCl)= ![]() ”Į
”Į
²Ł×÷¢Ś£ŗŃĪĖįµĪČė“æ¼īÖŠ£¬·¢Éś·“Ó¦£ŗ?
Na2CO3+HCl![]() NaCl+NaHCO3¢Ł?
NaCl+NaHCO3¢Ł?
NaHCO3+HCl![]() NaCl+CO2”ü+H2O¢Ś?
NaCl+CO2”ü+H2O¢Ś?
Ōņ·“Ó¦¢ŁĻūŗÄŃĪĖį£ŗ?
Éś³É0.100 mol NaHCO3£¬¹żĮæŃĪĖį (0.025 0 mol)ÓėNaHCO3·“Ӧɜ³É0.025 0 mol CO2”£ĖłŅŌ£ŗ
n¢Ł(CO2)”Ćn¢Ś(CO2)=0.062 5 mol”Ć0.025 0 mol=5”Ć2”£?
“š°ø£ŗA?



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
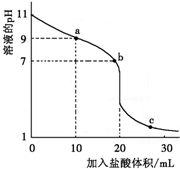 ŹŅĪĀĻĀ£¬½«0.100 0mol?L-1ŃĪĖįµĪČė20.00mL Ī“ÖŖÅØ¶ČµÄijŅ»ŌŖ¼īMOHČÜŅŗÖŠ£¬ČÜŅŗpHĖę¼ÓČėŃĪĖįĢå»ż±ä»ÆĒśĻßČēĶ¼ĖłŹ¾£®ĻĀĮŠÓŠ¹ŲĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
ŹŅĪĀĻĀ£¬½«0.100 0mol?L-1ŃĪĖįµĪČė20.00mL Ī“ÖŖÅØ¶ČµÄijŅ»ŌŖ¼īMOHČÜŅŗÖŠ£¬ČÜŅŗpHĖę¼ÓČėŃĪĖįĢå»ż±ä»ÆĒśĻßČēĶ¼ĖłŹ¾£®ĻĀĮŠÓŠ¹ŲĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗŗŚĮś½Ź”ŅĮ“ŗŹŠĀķÓĄĖ³ÖŠŃ§2012½ģøßČż11ŌĀŌĀæ¼»ÆѧŹŌĢā(ČĖ½Ģ°ę) ĢāŠĶ£ŗ013
|
¢Ł½«0.100 L””1.00 mol”¤L£1µÄ“æ¼īČÜŅŗÖšµĪµĪČė0.100 L””1.25 mol”¤L£1µÄŃĪĖįÖŠ£»¢Ś½«0.100 L””1.25 mol”¤L£1µÄŃĪĖįÖšµĪµĪČė0.100 L””1.00 mol”¤L£1µÄ“æ¼īČÜŅŗÖŠ£»Į½ÖÖ²Ł×÷²śÉśCO2µÄĢå»ż±ČĪŖ | |
| [””””] | |
A£® |
5”Ć2 |
B£® |
2”Ć5 |
C£® |
2”Ć1 |
D£® |
1”Ć1 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com