
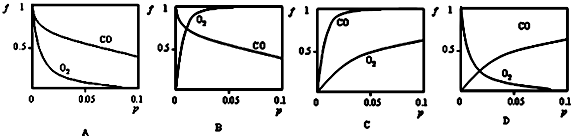

分析 (1)Mb(aq)+X(g)?MbX(aq),增大压强,平衡正向移动,因此无论是CO还是O2,随着压强的增大,结合率(f)都是逐渐增大;肌红蛋白与CO结合反应的平衡常数K(CO)远大于与O2结合的平衡常数K(O2),说明肌红蛋白与CO的结合能力比其与O2的结合能力强;
(2)①设平衡时吸附小分子的肌红蛋白(MbX)的浓度为[MbX],肌红蛋白(Mb)的浓度为[Mb],根据K的概念代入表达式;
②令Mb起始浓度为1,根据三段式:
Mb(aq)+O2(g)?MbO2(aq)
起始:1 0
转化:α α
平衡:1-α α
K=$\frac{c(Mb{O}_{2})}{c(Mb)•P({O}_{2})}$=$\frac{α}{(1-α)P({O}_{2})}$,根据图2,p(O2)=2.0kPa,α=80%,代入计算.
解答 解:(1)对于Mb(aq)+X(g)?MbX(aq),增大压强,平衡正向移动,因此无论是CO还是O2,随着压强的增大,结合率(f)都是逐渐增大.在常温下,肌红蛋白与CO结合反应的平衡常数K(CO)远大于与O2结合的平衡常数K(O2),说明肌红蛋白与CO的结合能力比其与O2的结合能力强,所以相同压强条件下,肌红蛋白与CO的结合率(f)更大,因此C图象符合,
故答案为:C;
(2)①设平衡时吸附小分子的肌红蛋白(MbX)的浓度为[MbX],肌红蛋白(Mb)的浓度为[Mb],则对于Mb(aq)+X(g)?MbX(aq),平衡常数K=$\frac{[MbX]}{[Mb]•\frac{p}{{p}_{0}}}$,所以[Mb]=$\frac{[MbX]}{K•\frac{p}{{p}_{0}}}$,所以吸附小分子的肌红蛋白(MbX)占总肌红蛋白的比例为$\frac{[MbX]}{[MbX]+[Mb]}$,将[Mb]代入整理可得,比例为$\frac{pK}{pK+{p}_{0}}$;
故答案为:$\frac{pK}{pK+{p}_{0}}$;
②令Mb起始浓度为1,根据三段式:
Mb(aq)+O2(g)?MbO2(aq)
起始:1 0
转化:α α
平衡:1-α α
K=$\frac{c(Mb{O}_{2})}{c(Mb)•P({O}_{2})}$=$\frac{α}{(1-α)P({O}_{2})}$,根据图2,p(O2)=2.0kPa,α=80%,K=$\frac{0.8}{(1-0.8)×2}$=2.00;
故答案为:2.00.
点评 本题考察化学反应原理的载体一改工业合成的惯例,采用人体中气体分子与蛋白结合的平衡模型,非常新颖.本题的思维含量很高,计算量也不小,特别是第(2)题要求对平衡常数的运算式熟练掌握,并且引入平衡分压概念,适当拓展,全面思考的能力.此题难度很大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
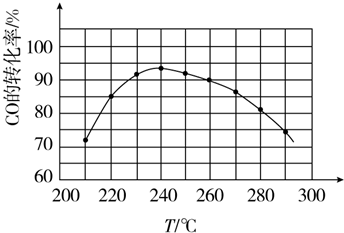
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/mol•L-1 | 0.64 | 0.50 | 0.50 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
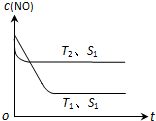 汽车尾气是城市的主要空气污染物,研究控制汽车尾气成为保护环境的首要任务.
汽车尾气是城市的主要空气污染物,研究控制汽车尾气成为保护环境的首要任务. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | I A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H | ||||
| 4 | J | K |
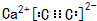 ,
,查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学式 | △H/(kJ?mol-1) | 化学式 | △H/(kJ?mol-1) |
| CO(g) | -283.0 | CH4(g) | -890.3 |
| H2(g) | -285.8 | CH3OH(l) | -726.5 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com