
A.常温时, 溶液的 溶液的 ,则该溶液中 ,则该溶液中 |
B. 溶液与 溶液与 溶液反应至中性的离子方程式为: 溶液反应至中性的离子方程式为: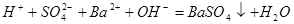 |
C.常温下物质的量浓度相等的下列四种溶液:① ;② ;② ;③ ;③ ;④ ;④ ,四种溶液中 ,四种溶液中 比较:② 比较:② ① ① ④ ④ ③ ③ |
D.常温下 的溶液: 的溶液: 、 、 、 、 、 、 可以常量共存 可以常量共存 |
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源:不详 题型:单选题
| A.四种溶液的pH大小顺序是③>②>①>④ |
| B.若分别加入25mL 0.1mol·L-1盐酸充分反应后,pH最大的是① |
| C.若将四种溶液稀释相同倍数,pH变化最大的是④ |
| D.升高温度,四种溶液的pH均减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.二者是同一反应 | B.两者没有任何联系 |
| C.盐类水解反应的逆反应是中和反应 | D.两者互为可逆反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.等于0.1mol/L | B.等于0.2mol/L |
| C.小于0.1mol/L | D.在0.1~0.2mol/L之间 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.④①③⑥③ | B.④③①⑥⑤③ | C.①③②⑥③ | D.④①③⑤⑥③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.pH相同的CH3COONa溶液、C6H5ONa溶液、Na2CO3溶液、NaOH溶液: c(CH3COONa)>c(C6H5ONa )>c(Na2CO3)>c(NaOH ) |
| B.将pH = 3的一元弱酸HA和pH = 11的NaOH溶液混合后溶液显碱性,一定有: c(H+) < c(OH- )< c(A-) <c(Na+) |
| C.在常温下,10 mL 0.02 mol·L-1 HCl溶液与10 mL 0.02 mol·L-1 Ba(OH)2溶液充分混合,体积为20 mL,则溶液的pH = 12+lg2 |
| D.将0.2 mol·L-1的盐酸与0.1 mol·L-1的NaAlO2溶液等体积混合,其溶液中离子浓度由小到大的顺序为:c(OH-)<c(Al3+)<c(H+)<c(Na+)<c(Cl-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 化学式 | 电离常数 |
| HClO | K=3×10-8 |
| H2CO3 | K1=4.3×10-7 |
| K2=5.6×10-11 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com