
����Ŀ����2017�����ʡТ���и����ϵ�һ��ͳ����ѧ�Ծ������ӷ�Ӧ�����������й㷺Ӧ�ã��������ӷ�Ӧ�ı�������Ҫ���塣��ش��������⣺
(1)����������K2S2O8��Һ�ڳ����»�ϣ��������õ���������(MnO2)����д���÷�Ӧ�����ӷ���ʽ_________________��
(2)��֪ij��Һ�п��ܺ���NO3����Cl-��SO42����CO32����NH4�� ��Fe3+��Al3+��K+�еļ��֣������������ӵ����ʵ�����ȡ�Ϊȷ������Һ�ijɷ֣�ijѧϰС����������ʵ�飺
��ȡ����Һ100mL���������NaOH��Һ�����ȣ��õ�0.02mol���壬ͬʱ�������ɫ�����������������ˡ�ϴ�ӡ����գ��õ�1.6g���壻����������Һ�м�������BaCl2��Һ���õ�4.66g����������ij�����
�����Һ�е�������Ϊ________________��������Ϊ_______________��
(3)������Ksp(AgCl)=1.8��10-10��Ksp(AgI)=1.0��10-16�����������£������͵�AgCl��Һ�ͱ��͵�AgI��Һ�������ϣ�________(��ᡱ���ᡱ)�г������ɡ�
(4)pH��ͬ����NH4Cl ��NH4Al(SO4)2 ��(NH4)2SO4������Һ��c(NH4�� )�ɴ�С˳��Ϊ________________(����ż���������=����������ʾ)��
���𰸡�
(1) S2O82-+Mn2++2H2O=MnO2+4H++2SO42-��
(2)NH4+��Fe3+��SO42-��NO3-��Cl-��
(3)�(4)��=��������
��������
���������(1)����������K2S2O8��Һ�ڳ����»�ϣ��������õ���������(MnO2)����Ӧ�����ӷ���ʽΪS2O82-+Mn2++2H2O=MnO2+4H++2SO42-���ʴ�Ϊ��S2O82-+Mn2++2H2O=MnO2+4H++2SO42-��
(2)ij��Һ���ܺ���NO3-��Cl-��SO42-��CO32-��NH4+��Fe3+��Al3+��K+����ȡ����Һ100mL���������NaOH��Һ�����ȣ��õ�0.02mol���壬ͬʱ�������ɫ��������ôһ�����ڣ�NH4+��Fe3+������ԭ���غ�֪��n(NH4+)=0.02mol���������ӹ���֪����Һ�в�����CO32-�������ˣ�ϴ�ӣ����գ��õ�1.6g����ΪFe2O3��n(Fe2O3)= ![]() =0.01mol������Feԭ���غ��n(Fe3+)=2n(Fe2O3)=0.02mol������������Һ�м�����BaCl2��Һ���õ�4.66g����������ij������ð�ɫ������BaSO4��n(BaSO4)=
=0.01mol������Feԭ���غ��n(Fe3+)=2n(Fe2O3)=0.02mol������������Һ�м�����BaCl2��Һ���õ�4.66g����������ij������ð�ɫ������BaSO4��n(BaSO4)= ![]() =0.02mol����������������غ��n(SO42-)=n(BaSO4)=0.02mol���������������ӵ����ʵ�����ȣ�����Һ�д��ڵ���غ㣬���ݵ���غ�֪���������������=0.02��3+0.02=0.08mol���������������=2��0.02mol=0.04mol��������Һ��һ��������������Cl-0.02mol��NO3-0.02mol���Ҳ����ܴ���Al3+��K+�����ݷ�������Һ��һ�����ڣ�NH4+��Fe3+��SO42-��NO3-��Cl-���ʴ�Ϊ��NH4+��Fe3+��SO42-��NO3-��Cl-��
=0.02mol����������������غ��n(SO42-)=n(BaSO4)=0.02mol���������������ӵ����ʵ�����ȣ�����Һ�д��ڵ���غ㣬���ݵ���غ�֪���������������=0.02��3+0.02=0.08mol���������������=2��0.02mol=0.04mol��������Һ��һ��������������Cl-0.02mol��NO3-0.02mol���Ҳ����ܴ���Al3+��K+�����ݷ�������Һ��һ�����ڣ�NH4+��Fe3+��SO42-��NO3-��Cl-���ʴ�Ϊ��NH4+��Fe3+��SO42-��NO3-��Cl-��
(3)���͵�AgCl��Һ�У�c(Ag+)=c(Cl-)=![]() =1.342��10-5�����͵�AgI��Һ�У�c(Ag+)=c(I-)=
=1.342��10-5�����͵�AgI��Һ�У�c(Ag+)=c(I-)=![]() =1.0��10-8���������Ϻ�Ũ�ȼ��룬c(Cl-)=6.71��10-6��c(I-)=5.0��10-9��c(Ag+)=6.71��10-6����Ϻ�Qc= c(Ag+)��c(I-)��Ksp(AgI)���� AgI�������ɣ��ʴ�Ϊ���
=1.0��10-8���������Ϻ�Ũ�ȼ��룬c(Cl-)=6.71��10-6��c(I-)=5.0��10-9��c(Ag+)=6.71��10-6����Ϻ�Qc= c(Ag+)��c(I-)��Ksp(AgI)���� AgI�������ɣ��ʴ�Ϊ���
(4)笠�����Ũ��Խ��ˮ�����Һ������Խǿ�������Ӻ���������Ӷ�笠����ӵ�ˮ����Ӱ�죬c(NH4�� )��=��������������笠����ӵ�ˮ�⣬����С���ʴ�Ϊ����=��������


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ԭ��Ӧ��2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)��Ƶ�ԭ�����ͼ��ʾ����ش��������⣺
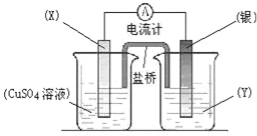
��1���缫X�IJ����� (��ѧʽ)���������ҺY�� ��
��2�����缫Ϊ��ص� ���������ĵ缫��ӦΪ ��X�缫�Ϸ����ĵ缫��ӦΪ ��
��3�����·�еĵ����Ǵ� �缫���� �缫��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ǿ���Ե���ɫ��Һ���ܴ������������������ ��
A��NH4+��Mg2+��SO42����Cl�� B��Ba2+��K+��OH����NO3��
C��Al3+��Cu2+��SO42����Cl�� D��Na+��Ca2+��Cl����HCO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л���ķ����������ǻ������ŵķ�Ӧ�����У���a��������Ӧ����b��ȡ����Ӧ����c��������Ӧ����d���ӳɷ�Ӧ����e��ˮ�ⷴӦ��������ȷ�������
A. ��a����b����c�� B. ��d����e�� C. ��b����d����e�� D. ��b����c����d����e��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȡ100mL 0.3molL��1��300mL 0.25molL��1������ע��500mL������ƿ�У���ˮϡ�����̶��ߣ��û����Һ��H+�����ʵ���Ũ���ǣ� ��
A.0.21 molL��1
B.0.56 molL��1
C.0.42 molL��1
D.0.26 molL��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ص����ʼ�ת����ϵ����ͼ��ʾ������B�ķ����к���һ������B������ʹ����ܷ���������Ӧ��C�Ĵ�����������Ǻϳɷ�ȩ��֬��ԭ��֮һ�����dz����ľ�����Ⱦ�E��ʹBr2��CCl4��Һ��ɫ��

(1)B�Ľṹ��ʽ��_____________________________��
(2)E��F�Ļ�ѧ����ʽ��___________________________��
(3)ijͬѧ����֤������ȫˮ��IJ���A����������ʵ������������Թ��м�������������Һ��������3��4 min���������������Ƶ�Cu(OH)2����Һ������������ϡ��������ȣ�������ȴ�μ�NaOH��Һ����Һ�ʼ��ԡ������ϲ���������ȷ��˳����(��ѡ�����)_____________��
A���٢ڢܢݢۢ� | B���٢ܢڢۢݢ� | C���٢ܢڢޢۢ� | D���٢ݢۢܢޢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������0.1molL��1NaCl��Һ�����в����ᵼ��������Һ�����ʵ���Ũ��ƫ�ߵ����� ��
A������ʱ�����̵ͣ����̸� B������ʱ���Ӷ�ȡ�̶�
C��ԭ����ƿϴ����δ���� D������ʱҺ�泬���˿̶���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(2015��������ۣ�3��6��)����˵������ȷ����( )
A��Na��H2O�ķ�Ӧ�������ķ��ȷ�Ӧ���÷�Ӧ���Է�����
B������Na2SO4��Һ��Ũ�������ʹ��������Һ������������ԭ����ͬ
C��FeCl3��MnO2���ɼӿ�H2O2�ֽ⣬ͬ�������¶��߶�H2O2�ֽ����ʵĸı���ͬ
D��Mg(OH)2��������Һ�д���ƽ�⣺Mg(OH)2(s) ![]() Mg2��(aq)��2OH��(aq)���ù��������NH4Cl��Һ
Mg2��(aq)��2OH��(aq)���ù��������NH4Cl��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I��������Ӳ�ȴ���ʴ������Ҫ�ĺϽ���ϡ�
��1����̬��ԭ�ӵļ۵��ӹ����ʾʽΪ________________��CrO2Cl2������Ϊ���ɫҺ�壬����CCl4���ܣ��ݴ��ж�CrO2Cl2�ľ�����������_________________��
��2�������CrCl3��6H2O����λ��Ϊ6���������ֲ�ͬ��ɡ���ͬ��ɫ�Ĺ��壬����һ��Ϊdz��ɫ���壬�ù�����������������Һ��Ӧʱ��0.5mol���������1mol�Ȼ���������������dz��ɫ�������������ȣ�Cl-��H2O��Ϊ_____________��
II.�黯��Ϊ�������뵼����ϣ������ṹ��ͼ��ʾ��

��3���黯�ؿ���(CH3)3Ga��AsH3��700���·�Ӧ�Ƶã���Ӧ�Ļ�ѧ����ʽΪ__________��
��4��AsH3���ӵ����幹��Ϊ__________������Asԭ�ӵ��ӻ���ʽ��______��1��(CH3)3Ga�����к���_________����������ĵ�һ������_______���>����<�����صĵ�һ�����ܡ�
��5���黯�ؾ���������ص����ԭ�Ӻ˼��Ϊa nm���黯�ص�Ħ������Ϊbg��mol-1�������ӵ�����ֵΪNA�����黯�ؾ�����ܶȱ���ʽ��_____________g��cm-3��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com