
| A、正十二面体 | B、正八面体 |
| C、正六面体 | D、正四面体 |
科目:高中化学 来源: 题型:
| A、④③②① | B、④③①② |
| C、③④①② | D、①③④② |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2mol、3mol |
| B、2mol、1mol |
| C、1.5mol、1.5mol |
| D、2.5mol、1.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、23 g钠在氧气中完全燃烧失电子数为0.5NA |
| B、46gNO2和N2O4混合气体中含有氮原子数为1NA~2NA |
| C、标准状况下,11.2L的SO3所含分子数为0.5 NA |
| D、室温下,16g甲烷含有共价键数为4 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、干冰气化时碳氧键发生断裂 |
| B、CaO和SiO2晶体中都不存在单个小分子 |
| C、K2O和K2O2中化学键类型完全相同 |
| D、苯分子中只有极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、摩尔是化学上常用的一个物理量 |
| B、某物质含有6.02×1023个微粒,含有这个数目微粒的物质一定是1mol |
| C、1摩尔氢气分子可以表示为1molH2 |
| D、硫酸的摩尔质量为98g |
查看答案和解析>>
科目:高中化学 来源: 题型:
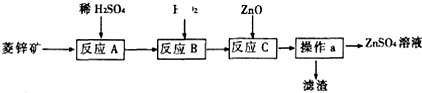
| 开始沉淀时的pH | 沉淀完全时的pH | |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.2 |
| Zn2+ | 6.2 | 9.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
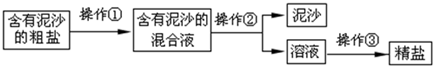
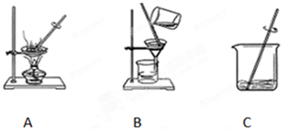
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com