
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | | | | ⑥ | | ⑦ | bl | |
| 三 | ① | ③ | ⑤ | | | | ⑧ | ⑩ |
| 四 | ② | ④ | | | | | ⑨ | |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
| A.粒子半径:Al3+>Mg2+>Na+ | B.热稳定性:HI>HBr>HCl>HF |
| C.酸性:H2CO3<H2SO4<HClO4 | D.碱性:Al(OH) 3>Mg(OH) 2>NaOH |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.X原子的电子层数比Y原子的电子层数多 |
| B.X的氢化物的沸点比Y的氢化物的沸点低 |
| C.X的气态氢化物比Y的气态氢化物稳定 |
| D.Y的单质能将X从NaX的溶液中置换出来 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
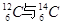 、②O2与O3、③正丁烷与异丁烷、④金刚石与石墨、⑤冰与水、⑥乙醇与二甲醚。请用序号填写对应的分类:(1)互为同位素的是 ;(2)互为同素异形体的是 ;(3)互为同分异构体的是 ;(4)属于同一化合物的是 。
、②O2与O3、③正丁烷与异丁烷、④金刚石与石墨、⑤冰与水、⑥乙醇与二甲醚。请用序号填写对应的分类:(1)互为同位素的是 ;(2)互为同素异形体的是 ;(3)互为同分异构体的是 ;(4)属于同一化合物的是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.元素周期表中有7个主族、7个副族 | B.碳元素位于第二周期IVA族 |
| C.稀有气体元素原子的最外层电子数均为8个 | D.氢分子中的化学键是共价键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com