
【题目】NO是治疗心血管疾病的信使分子,NO与空气接触的反应现象是______________
科目:高中化学 来源: 题型:
【题目】在一定条件下A2和B2可发生反应:A2(g)+3B2(g) ![]() 2AB3(g)。图1表示在一定温度下此反应过程中的能量变化,图2表示在固定容积为2L的密闭容器中反应时A2的物质的量随时间变化的关系,图3表示在其他条件不变的情况下,改变反应物B2的起始物质的量对此反应平衡的影响。下列说法错误的是
2AB3(g)。图1表示在一定温度下此反应过程中的能量变化,图2表示在固定容积为2L的密闭容器中反应时A2的物质的量随时间变化的关系,图3表示在其他条件不变的情况下,改变反应物B2的起始物质的量对此反应平衡的影响。下列说法错误的是

A. 该反应在低于某一温度时能自发进行
B. 10min内该反应的平均速率v(B2)=0.045mol/(L·min)
C. 11min时,其他条件不变,压缩容器容积至1L,n(A2)的变化趋势如图2中曲线d所示
D. 图3中T1<T2,b点对应状态下A2的转化率最高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】端炔烃在催化剂存在下可发生偶联反应,成为Glaser反应。
2R—C≡C—H![]() R—C≡C—C≡C—R+H2
R—C≡C—C≡C—R+H2
该反应在研究新型发光材料、超分子化学等方面具有重要价值。下面是利用Glaser反应制备化合物E的一种合成路线:

回答下列问题:
(1)D 的化学名称为__________,③的反应类型为_________。
(2)用1 mol E合成1,4-二苯基丁烷,理论上需要消耗氢气_______mol。
(3)写出反应④的化学方程式为_____________________________________。
(4)芳香化合物F是C的同分异构体,其分子中只有两种不同化学环境的氢,数目比为3:1,满足条件的同分异构体共有________种,写出其中任意1种的结构简式__________________________。
(5)写出用2-苯基乙醇为原料(其他无机试剂任选)制备化合物D的合成路线_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化锂(Li3N)常作固体电解质和催化剂,遇水蒸气剧烈反应生成氢氧化锂和氨气。某实验小组用一瓶氮气样品制备纯净的氮化锂的装置如图所示。

已知:连苯三酚碱性溶液能定量吸收少量O2,氯化亚铜盐酸溶液能定量吸收少量CO生成Cu(CO)Cl·H2O且易被O2氧化;在加热条件下,CO2与锂发生剧烈反应。下列说法正确的是
A. 干燥管e中试剂为无水CuSO4,用于检验氮气中的水蒸气
B. 为了减少气体用量,先点燃酒精灯再通入氮气
C. a、c中试剂分别为连苯三酚碱性溶液、浓硫酸
D. a装置可以换成盛装赤热铜粉的硬质玻璃管
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KClO3和浓盐酸在一定温度下反应会生成红黄色的易爆物二氧化氯。
(1)请完成该过程的化学方程式并配平。
____KClO3+___HCl(浓)===____KCl+____ClO2↑+____Cl2↑+___(_________)
(2)浓盐酸在反应中显示出来的性质是__(填写编号)。
①氧化性 ②还原性 ③酸性 ④碱性
(3)若反应生成0.1molCl2,则转移的电子数为__。
(4)ClO2具有很强的氧化性。因此,常被用作消毒剂,其消毒的效率(以单位质量得到的电子数表示)1kgClO2相当于___kgCl2。(提示:Cl2和ClO2在消毒过程中均变为Cl-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里用如图所示仪器和药品来制取纯净的无水氯化铜(Cu+Cl2![]() CuCl2)。图中A、B、C、D、E、F表示玻璃管接口,接口的弯曲和伸长等部分未画出。根据要求填写下列各小题空白。
CuCl2)。图中A、B、C、D、E、F表示玻璃管接口,接口的弯曲和伸长等部分未画出。根据要求填写下列各小题空白。

(1)如果所制气体从左向右流向时,上述各仪器装置的正确连接顺序是(填各装置的序号)(____)接(____)接(____)接(____)接(____)接(____),其中②与④装置相连时,玻璃管接口(用装置中字母表示)应是___接___。
(2)装置②的作用是___;装置④的作用是___。
(3)实验开始时,应首先检验装置的____,实验结束时,应先熄灭___处的酒精灯。
(4)在装置⑤的烧瓶中,发生反应的化学方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸银是中学实验室常用试剂。硝酸银不稳定,易发生如下反应:
①2AgNO3(s)= 2Ag(s)+ 2N02(g)+O2(g) △H1
②2NO2(g)![]() N2O4(g) △H2
N2O4(g) △H2
(1)2AgNO3(s)= 2Ag(s)+N2O4(g)+O2(g) △H=___________(用含△H1、△H2的式子表示)。
(2)实验室配制硝酸银溶液的操作方法是:将一定量硝酸银固体溶于浓硝酸中,加水稀释至指定体积。“硝酸”的作用是____________________________________________。
(3)一定温度下,在5L的恒容密闭容器中投入34 g AgNO3(s)并完全分解测得混合气体的总物质的量(n)与时间(t)的关系如图所示。
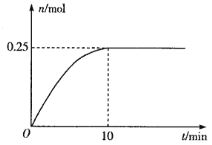
①下列情况能说明体系达到平衡状态的是___________(填字母)
a.Ag粉的质量不再改变 b.O2的浓度不再改变
c.NO2的体积分数不再改变 d.混合气体的密度不再改变
②反应开始到10min内N2O4的平均反应速率为___________mol·L-1·min-1。
③若达到平衡时,混合气体的总压强p=3.0MPa。在该温度下2NO2(g)![]() N2O4(g)的平衡常数Kp=___ (MPa)-1(结果保留2位小数)。[提示:用平衡时各组分分压替代浓度计算的平衡常数叫压强平衡常数(Kp),组分的分压(P1)=平衡时总压(P)×该组分的体积分数(
N2O4(g)的平衡常数Kp=___ (MPa)-1(结果保留2位小数)。[提示:用平衡时各组分分压替代浓度计算的平衡常数叫压强平衡常数(Kp),组分的分压(P1)=平衡时总压(P)×该组分的体积分数(![]() )]
)]
④达到平衡后,再向容器中充入少量的NO2,平衡2NO2(g)![]() N2O4(g)___________(填“向左”“向右”或“不”)移动,NO2的平衡转化率___________(填“增大”“减小”或“不变”)。
N2O4(g)___________(填“向左”“向右”或“不”)移动,NO2的平衡转化率___________(填“增大”“减小”或“不变”)。
(4)已知几种难溶物的溶度积如下表所示:
难溶物 | AgI | AgSCN | AgCl | Ag2CrO4 | Ag2S |
溶度积 | 8.5×10-17 | 1.2x10-12 | 1.8×10-10 | 1.1×10-11 | 6.7×10-50 |
颜色 | 黄色 | 白色 | 白色 | 红色 | 黑色 |
实验室常用AgNO3溶液滴定Cl-,宜选择___________作指示剂(填字母)
A.KI B. NH4SCN C. Na2CrO 4 D.K2S
(5)工业上,常用电解法精炼粗银。粗银中含有Cu、Au等杂质,用AgNO3溶液作电解质溶液。若以电流强度aA,通电bmin后,制得精银的质量为ckg,则该精炼装置的电流效率为___________(只要求列出计算式即可)。[已知:1mol电子带96500C(库仑)电量,电流效率等于阴极得电子数与通过电子总数之比]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去杂质,从而得到纯净的NaNO3晶体,相应的实验流程如图所示。

请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X___,沉淀A____。
(2)上述实验流程中①②③步均要进行的实验操作是___(填操作名称)。
(3)上述实验流程中加入过量Na2CO3溶液的目的是______________________________。
(4)按此实验方案得到的溶液3中肯定含有______(填化学式)杂质。为了解决这个问题,可以向溶液3中加入适量的___(填化学式),之后若要获得NaNO3晶体,需进行的实验操作是____(填操作名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a、b、c、X是中学化学中常见的四种物质,且a、b、c中含有同一种元素,其转化关系如下图所示。下列说法不正确的是
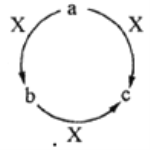
A. 若a、b、c均为厨房中常用的物质,则构成c中的阳离子半径小于其阴离子半径
B. 若a为一种气态氢化物,X为O2,则a分子中可能含有10个或者18个电子
C. 若b为一种两性氢氧化物,则X可能是强酸,也可能是强碱
D. 若a为固态非金属单质,X为O2,则O元素与a元素的原子序数之差可能为8
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com