
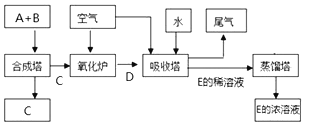
”¾ĢāÄæ”æĻĀĶ¼ĪŖij¹¤ŅµÉś²śµÄ»ł±¾Į÷³Ģ£¬ĘäÖŠA”¢BĪŖµ„ÖŹ£¬ĘäÓąĪŖ»ÆŗĻĪļ£¬ĒŅAŹĒÖŹĮæ×īĒįµÄĘųĢ唣ĘųĢåDŌŚ½ųČėĪüŹÕĖžŗó»įÓÉĪŽÉ«±äĪŖŗģ×ŲÉ«£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ĒėŠ“³öĖūĆĒµÄ»ÆѧŹ½£ŗ
C:___________E:___________
£Ø2£©ĪŖĮĖ¾”æÉÄܼõÉŁĪ²ĘųµÄÅÅ·Å£¬Ōņ½ųČėĪüŹÕĖžÄŚµÄĘųĢåDÓėæÕĘųµÄ×ī¼ŃĢå»ż±ČĪŖ_____________
£Ø3£©EµÄĻ”ČÜŅŗÓĆÖ±½ÓÕōĮóµÄ·½·ØŹĒĪŽ·ØµĆµ½70%ŅŌÉĻµÄÅØČÜŅŗµÄ£¬Ņņ“ĖĪŖĮĖĢįøßEČÜŅŗµÄÅØ¶Č£¬Ķس£ŌŚÕōĮóĖžÖŠ¼ÓČėŹŹĮæµÄĶŃĖ®¼Į”£Ōņ³£ÓĆÓŚ“ĖµÄĶŃĖ®¼ĮĪŖ£ŗ____________£ØÖ»ĢīŅ»ÖÖ¼“æÉ£©£¬øĆĶŃĖ®¼ĮµÄÓŵć»ņȱµćÓŠÄÄŠ©____________________”£
£Ø4£©ėēČā»ņÅŻ²ĖÖŠ»įŗ¬ÓŠ“óĮæµÄijÖĀ°©Īļ£¬ŹµŃéŹŅÖŠĪŖŃŠ¾æĘäŠŌÖŹ£¬æÉĄūÓĆDÓėijµ»ĘÉ«»ÆŗĻĪļ·“Ó¦ÖĘČ”øĆÖĀ°©Īļ£¬ŌņÖĘČ”Ź±·¢ÉśµÄ»Æѧ·“Ó¦·½³ĢŹ½ĪŖ_________________________£¬ČōøĆ·“Ó¦ÖŠÓŠ±źæöĻĀ4.48LD²ĪÓė·“Ó¦£¬Ōņ·“Ó¦¹ż³ĢÖŠ×ŖŅʵē×ÓŹżÄæŹĒ________________
”¾“š°ø”æ NH3 HNO3 4:15 ÅØĮņĖį ¶ŌŅĒĘ÷Éč±øøÆŹ“±Č½ĻŃĻÖŲ 2NO+Na2O2=2NaNO2 0.2NA£Ø»ņ1.204”Į1023£©
”¾½āĪö”æA”¢BĪŖµ„ÖŹ£¬ĘäÓąĪŖ»ÆŗĻĪļ£¬ĒŅAŹĒÖŹĮæ×īĒįµÄĘųĢ壬AŹĒĒāĘų”£ĘųĢåDŌŚ½ųČėĪüŹÕĖžŗó»įÓÉĪŽÉ«±äĪŖŗģ×ŲÉ«£¬Ņņ“ĖDŹĒNO£¬BŹĒµŖĘų£¬CŹĒ°±Ęų£¬EŹĒĻõĖį”£
£Ø1£©øł¾ŻŅŌÉĻ·ÖĪöæÉÖŖCŹĒNH3£¬EŹĒHNO3£»£Ø2£©øł¾Ż4NO+3O2+2H2O=4HNO3æÉÖŖNOÓėŃõĘųµÄ×ī¼ŃĢå»ż±ČŹĒ4£ŗ3£¬ŃõĘųŌŚæÕĘųÖŠŌ¼Õ¼20%£¬ĖłŅŌ½ųČėĪüŹÕĖžÄŚµÄĘųĢåNOÓėæÕĘųµÄ×ī¼ŃĢå»ż±ČĪŖ4:15£»£Ø3£©ÅØĮņĖį¾ßÓŠĶŃĖ®ŠŌ£¬Ņņ“Ė³£ÓĆÓŚ“ĖµÄĶŃĖ®¼ĮĪŖÅØĮņĖį£¬ÓÉÓŚÅØĮņĖį¾ßÓŠøÆŹ“ŠŌ£¬ĖłŅŌȱµćŹĒ¶ŌŅĒĘ÷Éč±øøÆŹ“±Č½ĻŃĻÖŲ£»£Ø4£©µ»ĘÉ«»ÆŗĻĪļŹĒ¹żŃõ»ÆÄĘ£¬ÓėNO·“Ӧɜ³ÉŃĒĻõĖįÄĘ£¬·½³ĢŹ½ĪŖ2NO+Na2O2=2NaNO2”£·“Ó¦ÖŠµŖŌŖĖŲ»ÆŗĻ¼Ū“Ó+2¼ŪÉżøßµ½+3¼Ū£¬Ź§Č„1øöµē×Ó”£4.48L±ź×¼×“æöĻĀNOŹĒ0.2mol£¬ĖłŅŌ·“Ó¦¹ż³ĢÖŠ×ŖŅʵē×ÓŹżÄæŹĒ0.2NA”£


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĶłNa2S”¢Na2SO3µÄ»ģŗĻĪļÖŠ¼ÓČėĻ”ĮņĖį£¬·“Ó¦ÖŠ²»æÉÄÜÉś³ÉµÄĪļÖŹŹĒ
A.SB.SO2C.H2SD.SO3
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĶ¬ĪĀĶ¬Ń¹ĻĀ£¬¼×”¢ŅŅĮ½ČŻĘ÷·Ö±šŹ¢ÓŠ¼×Ķé(CH4)ĘųĢåŗĶ°±Ęų(NH3)£¬ŅŃÖŖĖüĆĒĖłŗ¬Ō×ÓøöŹżĻąĶ¬£¬Ōņ¼×”¢ŅŅĮ½ČŻĘ÷µÄĢå»ż±ČĪŖ
A. 4 £ŗ5 B. 5 £ŗ4 C. 4 £ŗ3 D. 1 £ŗ1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĶā½ēŅņĖŲ¶Ō»Æѧ·“Ó¦ĖŁĀŹæÉÄÜĪŽÓ°ĻģµÄŹĒ
A.Ń¹ĒæB.ĪĀ¶ČC.ÅضČD.“߻ƼĮ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŗ£“ųÖŠŗ¬ÓŠ·įø»µÄµā£®ĪŖĮĖ“Óŗ£“ųÖŠĢįČ”µā£¬Ä³ŃŠ¾æŠŌѧĻ°Š”×éÉč¼Ę²¢½ųŠŠĮĖŅŌĻĀŹµŃé£ŗ 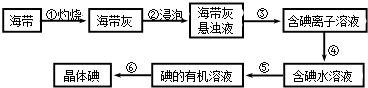
£Ø1£©²½Öč¢ŪµÄŹµŃé²Ł×÷Ćū³ĘŹĒ£»²½Öč¢ŽµÄÄæµÄŹĒ“Óŗ¬µā±½ČÜŅŗÖŠ·ÖĄė³öµ„ÖŹµāŗĶ»ŲŹÕ±½£¬øĆ²½ÖčµÄŹµŃé²Ł×÷Ćū³ĘŹĒ £®
£Ø2£©²½Öč¢ÜŠč¼ÓČėµÄŹŌ¼ĮŹĒ £¬ ·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ £®
£Ø3£©²½Öč¢ŻÖŠ£¬Ä³Ń§ÉśŃ”ŌńÓƱ½Ą“ĢįČ”µā£¬ĄķÓÉŹĒ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»¶ØĢõ¼žĻĀĻõĖįļ§ŹÜČČ·Ö½āµÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ5NH4NO3£½2HNO3£«4N2£«9H2O£¬ŌŚ·“Ó¦ÖŠ±»Ńõ»ÆÓė±»»¹ŌµÄµŖŌ×ÓŹżÖ®±ČĪŖ
A. 3”Ć5 B. 5”Ć4 C. 1”Ć1 D. 5”Ć3
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠø÷×éĘųĢåÖŠ£¬Ķس£ĒéæöĻĀÄܹ²“ę£¬²¢¶¼ÄÜÓĆÅØĮņĖįŗĶ¼īŹÆ»ŅøÉŌļµÄŹĒ
A.SO2£¬H2S£¬O2B.NH3£¬H2£¬N2
C.N2£¬H2£¬COD.HCl£¬Cl2£¬CO2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄ³ŃŠ¾æŠŌѧĻ°Š”×齫ĻĀĮŠ×°ÖĆČēĶ¼Į¬½Ó£¬C”¢D”¢E”¢F”¢X”¢Y ¶¼ŹĒ¶čŠŌµē¼«£®½«µēŌ“½ÓĶØŗó£¬ĻņŅŅÖŠµĪČė·ÓĢŖŹŌŅŗ£¬ŌŚF¼«ø½½üĻŌŗģÉ«£®ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ 
£Ø1£©µēŌ“A ¼«µÄĆū³ĘŹĒ£ØÕż¼«»ņøŗ¼«£©£®
£Ø2£©¼××°ÖĆÖŠµÄC¼«µÄµē¼«·“Ó¦Ź½ £®
£Ø3£©ÓūÓƱū×°ÖĆøųĶ¶ĘŅų£¬GÓ¦øĆŹĒ£ØĢī”°Ķ”±»ņ”°Ņų”±£©£¬µē¶ĘŅŗµÄÖ÷ŅŖ³É·ÖŹĒ£ØĢī»ÆѧŹ½£©£®
£Ø4£©×°Öƶ”ÖŠµÄĻÖĻóŹĒ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĢå»żĪŖV mL£¬ĆܶČĪŖd g/mL£¬ČÜÖŹµÄĦ¶ūÖŹĮæĪŖM g”¤mol-1£¬ĪļÖŹµÄĮæÅضČĪŖc mol”¤L-1£¬ČÜÖŹµÄÖŹĮæ·ÖŹżĪŖa%£¬ČÜÖŹµÄÖŹĮæĪŖm g”£ĻĀĮŠŹ½×ÓÕżČ·µÄŹĒ
A. m=a V/(100d) B. c=1000da/M
C. c=1000m/(VM) D. a%=[cM/(1000d)]%
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com