
分析 (1)ZnS是不溶于水的白色沉淀;
(2)CuS是黑色沉淀,比ZnS更难溶;
(3)①Zn2+与S2-反应生成ZnS沉淀;
②是沉淀转化,ZnS沉淀转化为CuS沉淀;
(4)据CuS的Ksp和其Qc的大小比较分析.
解答 解:(1)ZnS不溶于水,向ZnSO4溶液中滴加Na2S溶液,会生成白色沉淀ZnS,故答案为:生成白色沉淀;
(2)向白色沉淀ZnS中滴加适量的0.1 mol•L-1的CuSO4溶液时,白色沉淀逐渐溶解,生成黑色沉淀CuS,故答案为:白色沉淀逐渐溶解,生成黑色沉淀;
(3)①向ZnSO4溶液中滴加Na2S溶液,会生成白色沉淀ZnS,反应的了离子方程式为Zn2++S2-=ZnS↓,故答案为:Zn2++S2-=ZnS↓;
②向白色沉淀ZnS中滴加适量的0.1 mol•L-1的CuSO4溶液时,白色沉淀逐渐溶解,生成黑色沉淀CuS,反应的离子方程式为Cu2+(aq)+ZnS(s)=CuS(s)+Zn2+(aq),
故答案为:Cu2+(aq)+ZnS(s)=CuS(s)+Zn2+(aq);
(4)ZnS饱和溶液中存在沉淀的溶解平衡,向白色沉淀ZnS中滴加适量的0.1 mol•L-1的CuSO4溶液时,c(Cu2+)•c(S2-)>Ksp(CuS),能够生成CuS沉淀,c(S2-)减小,促进ZnS溶解平衡正向移动,ZnS逐渐溶解,
故答案为:向ZnS沉淀中加入CuSO4溶液时,c(Cu2+)•c(S2-)>Ksp(CuS),能够生成CuS沉淀,c(S2-)减小,ZnS逐渐溶解.
点评 本题考查了沉淀的生成和转化,注意沉淀容易转化为更难溶的沉淀,题目难度不大.


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:填空题
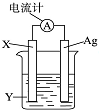 依据氧化还原反应:2Ag++Cu═Cu2++2Ag设计的原电池如图所示.请回答下列问题:
依据氧化还原反应:2Ag++Cu═Cu2++2Ag设计的原电池如图所示.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径 Z>Y>X | |
| B. | Z的非金属性最强 | |
| C. | 氢化物还原性XH3>H2Y>HZ,稳定性XH3>H2Y>HZ | |
| D. | 最高氧化物对应水化物H3XO4酸性最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com