
硫酸的产量常常被用做衡量一个国家工业发展水平的标志。下列有关硫酸的性质和使用的叙述中错误的是( )。
A.可以选用铁罐车储运浓硫酸
B.盛装浓硫酸的试剂瓶应印有如图所示的警示标记

C.稀释浓硫酸时应将浓硫酸慢慢注入水中
D.泄漏在水沟中的浓硫酸可以用生石灰进行掩埋
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
如图是一个用铂丝作电极,电解稀的MgSO4溶液的装置,电解液中加有中性红指示剂,此时溶液呈红色。(指示剂的pH变色范围:6.8~8.0,酸色—红色,碱色—黄色)回答下列问题:
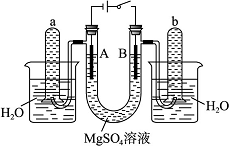
(1)下列关于电解过程中电极附近溶液颜色变化的叙 述正确的是______(填编号);
述正确的是______(填编号);
①A管溶液由红变黄
②B管溶液由红变黄
③A管溶液不变色
④B管溶液不变色
(2)写出 A管中发生反应的反应式:____________________________________________; (3)写
A管中发生反应的反应式:____________________________________________; (3)写 出B管中发生反应的反应式:____________________________________________;
出B管中发生反应的反应式:____________________________________________;
(4)检验a管中气体的方法是_ __________________________________________________;
(5)检验b管中气体的方法是_________________________________________________;
(6)电解一段时间后,切断电源,将电解液倒入烧杯内观察到的现象是________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
铵盐是一类重要的氮的化合物,设NA表示阿伏加德罗常数的值,下列叙述正确的是 ( )。
A.1 mol NH4+含有的电子数为11NA
B.NH4+中N元素的化合价为-3,在氧化还原反应中常作氧化剂
C.0.1 L 3 mol·L-1的NH4NO3溶液中氮原子数等于0.6NA
D.硫酸铵中既含有离子键,又含有共价键,而氯化铵中只含有离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
硝酸是极其重要的化工原料,工业上将产生的NO2在密闭容器中用水多次反复循环吸收制备硝酸。
(1)工业上用水吸收NO2生产HNO3,生成的气体经多次氧化、吸收的循环操作充分转化为硝酸(假定上述过程无其他损失)。试写出上述反应的化学方程式:
_________________________________________________________________
___________________________________ _____________________________________。
_____________________________________。
(2)为了证明NO也可以与氧气和水共同反应生成HNO3,某学生设计了如图所示装置(有关夹持装置已略去)。
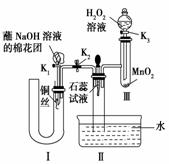
①检查装置气密性良好后,为观察到NO气体生成,打开K1,关闭K2,应从U形管的长管口注入稀硝酸至________后,迅速关闭K1,观察到U形管内的现象是____________
________________________________________________________________________。
②装置Ⅲ中发生反应的化学方程式为________________________________。
③蘸NaOH溶液的棉花团的作用是________________________________________。
④打开K2,至装置Ⅱ中长玻璃管中的气体呈无色后,打开K3,反应一段时间后,长玻璃管中并 未充满液体。设计简单方法检验长玻璃管中的气体是否含NO_____________
未充满液体。设计简单方法检验长玻璃管中的气体是否含NO_____________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
中学化学中几种常见物质的转化关系如下图(部分产物未列出)。A是一种金属单质,D是一种非金属固体单质。
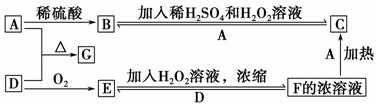
请回答下列问题:
(1)A、C的化学式分别为A________,C________。
(2)F的浓溶液与A反应过程中,F体现的性质与下列反应中H2SO4体现的性质完全相同的是________。
A.C+2H2SO4(浓)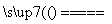 CO2↑
CO2↑ +2SO2↑+2H2O
+2SO2↑+2H2O
B.Fe+H2SO4===FeSO4+H2↑
C.Cu+2H2SO4(浓)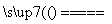 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
D.FeO+H2SO4===FeSO4+H2O
(3)写出反应E+H2O2―→F的化学方程式:________。
(4)若反应F+D―→E转移电子数为6.02×1023,则消耗D的质量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
水是一种宝贵的自然资源。
(1)生活污水中,常含N、P化合物而造成水体植物富营养化污染。水中的氨在微生物的作用下,可发生以下一系列变化:A、 NH3 + O2 →HNO2+ H2O(未配平)
B、2HNO2+O2 → 2HNO3,回答以下问题
① 配平反应A并标出电子转移的方向与数目:
____NH3+ ___O2 → ___HNO2+ ____ H2O
② 反应B中被氧化的元素是 。
(2)氧化还原法是处理污水常用的方法之一。某工厂排放的污水,经检测,污水中含有
0.012 mol/L的游离态溴,可用Na2SO3还原除去污水中的溴,请写出其离子方程式:
若处理5L这种污水,至少需加入0.05mol/L的Na2SO3溶液 L才能将单质溴全部除去。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中属于取代反应的是( )
①由乙醇制备乙烯 ②乙酸和乙醇反应制备乙酸乙酯 ③丙烯和溴的四氯化碳溶液反应
④苯和浓硝酸、浓硫酸共热 ⑤乙酸乙酯和稀硫酸共热 ⑥溴乙烷和氢氧化钠的水溶液共热
A.①②④⑤ B.②④⑤⑥ C.②③④⑤ D.①③⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com