
| A、甲烷 | B、氨气 |
| C、甲醛 | D、二氧化硫 |
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:
| A、臭氧是饮用水的理想消毒剂之一,因为它杀菌能力强又不影响水质 |
| B、向含有Hg2+的废水中加入Na2S,可使Hg2+浓度降到几乎对人体无害 |
| C、食品包装袋中常放人小袋的生石灰,目的是防止食品氧化变质 |
| D、提倡使用无氟冰箱,主要是为了保护大气臭氧层 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4+的数目 |
| B、OH-的物质的量浓度 |
| C、NH4+的物质的量浓度 |
| D、H+的物质的量浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+ Na+ SO42- CO32- |
| B、NH4+ Mg2+ NO3- Cl- |
| C、Na+ K+ HCO3- Cl- |
| D、K+ Na+ AlO2- NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cl2只作氧化剂 |
| B、Cl2只作还原剂 |
| C、Cl2既作氧化剂又作还原剂 |
| D、氯元素的化合价不发生变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
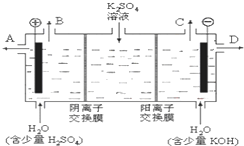
 Na2CO3是一种很重要的化学物质,某学生拟在实验室中制备Na2CO3.下面是他的制备实验过程:用50mL NaOH溶液吸收CO2气体,制备Na2CO3溶液.为了防止通入的CO2气体过量,生成NaHCO3,他设计了如下实验步骤:
Na2CO3是一种很重要的化学物质,某学生拟在实验室中制备Na2CO3.下面是他的制备实验过程:用50mL NaOH溶液吸收CO2气体,制备Na2CO3溶液.为了防止通入的CO2气体过量,生成NaHCO3,他设计了如下实验步骤:查看答案和解析>>
科目:高中化学 来源: 题型:
| 浓度 物质 | CO | H2O | CO2 | H2 |
| 起始浓度/(mol?L-1) | 2.0 | x | 0 | 0 |
| 平衡浓度/(mol?L-1) | 0.4 | 6.4 | 1.6 | 1.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
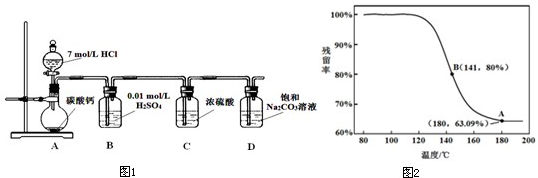
| 剩余固体的物质 |
| 原始固体的物质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com