
在T ℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。
又知T ℃时,AgCl的Ksp=4×10-10,下列说法不正确的是( )
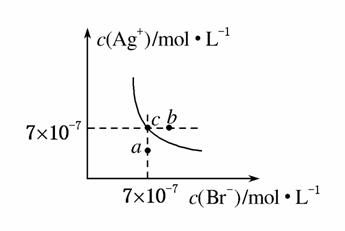
A.在T ℃时,AgBr的Ksp为4.9×10-13
B.图中b点对应的是向AgBr饱和溶液中加入NaBr固体后的溶液
C.图中a点对应的是AgBr的不饱和溶液
D.AgCl沉淀能较容易转化为AgBr沉淀
科目:高中化学 来源: 题型:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0”刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放出25.00mL待测溶液到锥形瓶中。
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol·L-1标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0”刻度以下的位置,记下读数。
③向锥形瓶中滴入酚酞作指示剂,进行滴定。滴定至终点,测得所耗盐酸的体积为V1mL。
④重复以上过程,但在滴定过程中向锥形瓶中加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL。
试回答下列问题:

(1)滴定终点时的现象为锥形瓶中的溶液
由_____________________________________________;
(2)滴定时边滴边摇动锥形瓶,眼睛应观察
________________________________________________;
(3)该小组在步骤①中的错误是________________________,由此造成的测定结果________(填“偏高”或“偏低”或“无影响”);
(4)步骤②缺少的操作是____________________________;
(5)如上图是某次滴定时的滴定管中的液面,其读数为___mL;
(6)根据下列数据:
| 测定次数 | 待测液体积/mL | 标准盐酸体积/mL | |
| 滴定前读数/mL | 滴定后读数/mL | ||
| 第一次 | 25.00 | 0.40 | 20.38 |
| 第二次 | 25.00 | 4.00 | 24.02 |
请计算待测烧碱溶液的物质的量浓度。(请写出解答过程)
查看答案和解析>>
科目:高中化学 来源: 题型:

室温下,抽去如图所示装置中的玻璃片,使两种气体充分反应(整个过程中认为装置气密性良好,上下两个集气瓶的容积分别为1.2V L、VL)。下列说法正确的是( )
A.反应后各瓶内压强均是反应前的1/10
B.装置中氢元素的总质量为0.42 g
C.生成物的分子总数为0.1NA
D.体系内自发地进行了一种熵减、焓增的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
在一密闭容器中发生反应:2X(g)+Y(g)aZ(g) ΔH=Q kJ·mol-1,开始按体积比2:1将X、Y充入反应器中,一定条件下发生反应。图甲和图乙是根据反应绘制的图象,下列有关说法正确的是( )
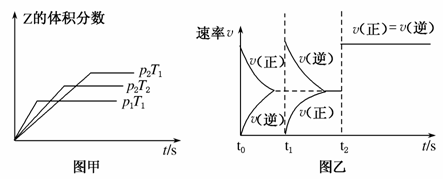
A.图甲,p1>p2,a<3
B.图甲,T1<T2,Q>0
C.图乙,t1时表示恒温、恒压条件下,向平衡体系中充入一定量的Z气体
D.图乙,如果a=3,t2时表示向体系中加入了催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25 ℃时有关弱酸的电离平衡常数如下表:
| 弱酸化学式 | HX | HY | H2CO3 |
| 电离平衡常数 | 7.8×10-9 | 3.7×10-15 | K1=4.3×10-7 K2=5.6×10-11 |
下列推断正确的是( )
A.HX、HY两种弱酸的酸性:HX>HY
B.相同条件下溶液的碱性:NaX>Na2CO3>NaY>NaHCO3
C.结合H+的能力:CO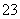 >Y->X->HCO
>Y->X->HCO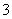
D.HX和HY酸性相同,都比H2CO3弱
查看答案和解析>>
科目:高中化学 来源: 题型:
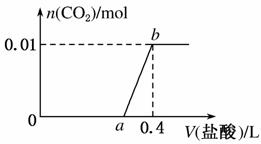
向NaOH和Na2CO3混合溶液中滴加0.1 mol·L-1稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示。下列判断正确的是( )
A.在0~a范围内,只发生中和反应
B.ab段发生反应的离子方程式为:CO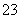 +2H+===CO2↑+H2O
+2H+===CO2↑+H2O
C.a=0.3
D.原混合溶液中NaOH与Na2CO3的物质的量之比为1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
根据Fe3++AgFe2++Ag+,可用Fe3+做刻蚀液将试管中的银镜洗去。
(1)FeCl3溶液显酸性,原因是________(用离子方程式表示)。
(2)关于FeCl3溶液洗银后的相关叙述正确的是________(填选项字母)。
a.铁元素质量减小 b.c(Fe3+)减小
c.c(Cl-)不变
(3)用Fe(NO3)3溶液洗银后,某同学欲从洗银废液(含Fe3+、Fe2+、Ag+、NO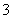 )中回收银,设计了如下路线:
)中回收银,设计了如下路线:
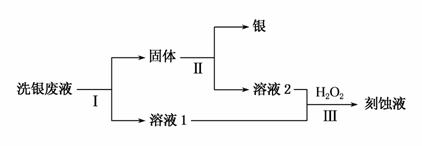
①过程Ⅰ中反应的离子方程式是__________________________。
②过程Ⅱ中加入的试剂可以是_____________________。
③过程Ⅲ中发生反应的离子方程式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于热化学反应的描述中正确的是( )
A.HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热
△H=2×(-57.3)kJ/mol
B.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)===2CO(g)+O2(g)反应的
△H=+2×283.0kJ/mol
C.△H>0,△S>0,在任何温度下都不可自发进行。
D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com