
【题目】石油产品中除含有H2S外,还含有各种形态的有机硫,如COS、CH3SH等。
回答下列问题:
(1)CH3SH(甲硫醇)的电子式为__________。
(2)CO和H2S反应可产生羰基硫( COS)。在一恒容密闭容器中发生反应:CO(g)+H2S(g)![]() COS(g)+H2(g)并达到平衡,数据如下表所示:
COS(g)+H2(g)并达到平衡,数据如下表所示:
实验 | 温度/℃ | 起始时 | 平衡时 | |||
n(CO)/mol | n(H2S)/mol | n(COS)/mol | n(H2)/mol | n(CO)/mol | ||
1 | 150 | 10.0 | 10.0 | 0 | 0 | 7.0 |
2 | 150 | 7.0 | 8.0 | 2.0 | 4.5 | a |
3 | 400 | 20.0 | 20.0 | 0 | 0 | 16.0 |
①该反应是________反应(填“吸热”或“放热”)。
②实验1达平衡时,CO的转化率为_______。
③实验2达到平衡时,a_______7.0(填“大于”“小于”或“等于”)。
④实验3达平衡后,再充入1.0 molH2,平衡常数值____(填“增大”“减小”或“不变”)。
(3)COS是大气污染物。在酸性溶液中可用H2O2氧化COS生成一种强酸脱硫。该脱除反应的化学方程式为_______________。
(4)有一种脱硫工艺为:真空K2CO3一克劳斯法。
①K2CO3溶液吸收H2S的反应为K2CO3 +H2S =KHS +KHCO3,该反应的平衡常数的对数值为lgK=_____(已知:H2CO3 lgK1=-6.4,lgK,2=- 10.3;H2S lgKl=-7.0,lgK
②已知下列热化学方程式:
a. 2H2S(g)+3O2(g)=2SO2(g)+2H2O(1) △H1=-1172kJ/mol
b. 2H2S(g)+O2(g)=2S(s)+2H2O(1) △H2 = 632 kJ/mol
克劳斯法回收硫的反应为SO2和H2S气体反应生成S(s),则该反应的热化学方程式为_________。
【答案】  放热 30% 小于 不变 COS + 4H2O2 = CO2 + H2SO4+ 3H2O 3. 3 2H2S (g) +SO2 (g) =3S (s) +2H2O (1) △H=-362kJ/mol
放热 30% 小于 不变 COS + 4H2O2 = CO2 + H2SO4+ 3H2O 3. 3 2H2S (g) +SO2 (g) =3S (s) +2H2O (1) △H=-362kJ/mol
【解析】(1)CH3SH (甲硫醇)是共价化合物,硫原子形成两个共价键,碳原子形成四个共价键,电子式为;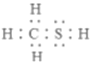 ,故答案为:
,故答案为: ;
;
(2)①实验1和实验3,如果温度不变,平衡时实验的n(CO)=7.0×2=14mol,而现在是16mol,说明升高温度平衡逆向移动,逆反应是吸热,正反应是放热,故答案为:放热;
②CO的转化率为![]() ×100%=30%,故答案为:30%;
×100%=30%,故答案为:30%;
③150℃,K=![]() =
=![]() ,而Qc=
,而Qc=![]() =
=![]() ,即Qc<K,反应向正反应方向移动,所以实验2达平衡时,a<7.0,故答案为:小于;
,即Qc<K,反应向正反应方向移动,所以实验2达平衡时,a<7.0,故答案为:小于;
④K是温度的函数,温度不变K不变,而充入1.0 mol H2,所以K值不变,故答案为:不变;
(3)在酸性溶液中,H2O2氧化COS生成一种强酸为硫酸,反应的化学方程式为COS + 4H2O2 = CO2 + H2SO4+ 3H2O,故答案为:COS + 4H2O2 = CO2 + H2SO4+ 3H2O;
(4)①K2CO3溶液吸收H2S的反应为K2CO3+H2S=KHS+KHCO3,该反应的平衡常数K=![]() =
=![]() ,lgK=LgKa1(H2S)-lgKa2(H2CO3)=-7-(-10.3)=3.3,故答案为:3.3;
,lgK=LgKa1(H2S)-lgKa2(H2CO3)=-7-(-10.3)=3.3,故答案为:3.3;
②a.2H2S(g)+3O2(g)═2SO2(g)+2H2O(l)△H1=-1172kJ/mol,b.2H2S(g)+O2(g)═2S(s)+2H2O(l) △H2=-632 kJ/mol,盖斯定律计算(b×3-a)×![]() 得到克劳斯法回收硫的反应为SO2和H2S气体反应生成S(s)反应的热化学方程式:2H2S(g)+SO2(g)=3S(s)+2H2O(l)△H=-362 kJmol-1,故答案为:2H2S(g)+SO2(g)=3S(s)+2H2O(l)△H=-362kJmol-1。
得到克劳斯法回收硫的反应为SO2和H2S气体反应生成S(s)反应的热化学方程式:2H2S(g)+SO2(g)=3S(s)+2H2O(l)△H=-362 kJmol-1,故答案为:2H2S(g)+SO2(g)=3S(s)+2H2O(l)△H=-362kJmol-1。


科目:高中化学 来源: 题型:
【题目】根据问题填空:
(1)氟化氢水溶液中存在的氢键有种;分子(CN)2中键与键之间的夹角为180°,并有对称性,分子中每个原子最外层均满足8电子稳定结构,其结构式为 , 1个分子中含有个π键;
(2)金属镍及其化合物在合金材料以及催化剂等方面应用广泛,NiO的晶体结构类型与氯化钠的相同,NiO晶胞中Ni和O的配位数均为;很多不饱和有机物在Ni催化下可以H2发生加成反应,如①CH2=CH2、②HC≡CH、③ ![]() 、④HCHO等,其中碳原子不是采取sp2杂化的分子有(填物质编号),HCHO分子的立体构型为 .
、④HCHO等,其中碳原子不是采取sp2杂化的分子有(填物质编号),HCHO分子的立体构型为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用溴和苯反应制取溴苯,得到粗溴苯后,要用如下操作精制:
①蒸馏;②水洗;③用干燥剂干燥;④10%NaOH溶液洗;⑤水洗。
正确的操作顺序是
A. ①②③④⑤ B. ④②③①⑤ C. ②④①⑤③ D. ②④⑤③①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质能发生消去反应且产物只有一种的是 ( )
A.CH3CHICH2 CH3 B.CH3OH C.(CH3)3COH D.(CH3)3C—CH2C1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组要完成中和热的测定.回答下列问题:
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5molL﹣1盐酸、0.55molL﹣1NaOH溶液,实验尚缺少的玻璃用品是 .
(2)已知:反应后溶液的比热容c为4.18J℃﹣1g﹣1 , 0.5molL﹣1盐酸和0.55molL﹣1NaOH溶液的密度均为1gcm﹣3 . 实验时记录的实验数据如表:
实验 | 反应物及用量 | 溶 液 温 度 | ||
t1 | t2 | |||
1 | 50mL0.55molL﹣1NaOH溶液 | 50mL.0.5molL﹣1HCl溶液 | 20℃ | 23.3℃ |
2 | 50mL0.55molL﹣1NaOH溶液 | 50mL.0.5molL﹣1HCl溶液 | 20℃ | 23.5℃ |
①盐酸和氢氧化钠反应的中和热△H1=(保留两位小数)
②已知:CH3COOH(aq)CH3COO﹣(aq)+H+(aq)△H2>0,
CH3COOH(aq)+OH﹣(aq)=CH3COO﹣(aq)+H20(l)△H3 则△H3△H1(填“>”、“<”、“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①甲烷、②乙烷、③乙烯、④苯、⑤甲苯、⑥二甲苯、⑦乙醇、⑧乙酸、
⑨葡萄糖,它们都是常见的重要化工原料。
(1)上述物质中,氢元素的质量分数最大的是________(填分子式);
(2)分别写出⑦、⑧中所含官能团的名称__________、___________,
二者发生酯化反应的化学方程式______________________________________,
如果用4.6 g乙醇和9.0 g乙酸充分反应制得乙酸乙酯5.28 g,则本实验的产率是:__________(产率指的是目标生成物的实际产量与理论产量的比值)。
(3)上述物质中,能发生加成反应的烃类物质有:_______________(填序号)。
(4)下列物质中,不能通过乙烯加成反应得到的是____(填序号)。
a. CH3CH3 b. CH3CHCl2 c. CH3CH2Br
(5)聚氯乙烯,简称PVC,这种材料如果用于食品包装,它对人体的安全性有一定的影响,写出生产聚氯乙烯的化学方程式:__________________________
(6)苯、甲苯、二甲苯是用途广泛的有机溶剂。二甲苯的结构有______种,其中一种被称为“PX”,它的一氯代物只有两种,则“PX”的结构简式是______________。
(7)写出乙醇催化氧化反应的化学方程式 _________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有通电条件下,用如图所示装置由乙二醛(OHC-CHO)制备乙二酸(HOOC-COOH),其反应为:OHC-CHO+2Cl2+2H2O![]() HOOC-COOH+4HCl。下列说法正确的是
HOOC-COOH+4HCl。下列说法正确的是
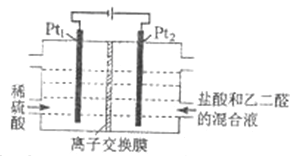
A. Pt1的电极反应为:2H2O+ 2e-=2OH-+H2↑
B. 盐酸起提供Cl- 和增强导电性的作用
C. 每消耗0.1mol乙二醛,在Pt1极放出2.24 L 气体(标准状况)
D. 每得到1mol乙二酸将有2 mol H+从右室迁移到左室
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辣椒素是辣椒的活性成分,可在口腔中产生灼烧感,能够起到降血压和胆固醇的功效,进而在很大程
度上预防心脏病,也能缀解肌肉关节疼痛。辣椒素酯类化合物的结构可以表示为:
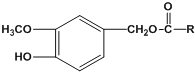
其中一种辣椒素脂类化合物J的合成路线如下:
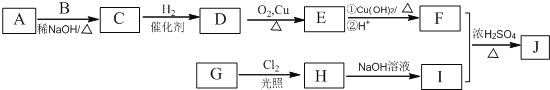
已知:①A、B和E为同系物,其中B的相对分子质量为44,A和B核磁共振氢谱显示都有两组峰
②J的分子式为C15H22O4
③![]()
回答下列问题:
(1)G所含官能团的名称为_______________________。
(2)由A和B生成C的化学方程式为___________________。
(3)由C生成D的反应类型为____________,D的化学名称为________________。
(4)由H生成I的化学方程式为_______________________。
(5)在G的同分异构体中,苯环上的一氯代物只有种的共有_____种(不含立体异构),其中核磁共振氢谱显示两组峰的是__________(写结构简式)。
(6)参照上述路线,设计一条以乙醛为原料(无机试剂任选)合成乙酸正丁酯的路线:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是一种重要的基本化工原料,其产量可以用来衡量一个国家的石道化工发展水平。E是具有香味的液体。转化关系如下图所示(部分反应条件产物省略):
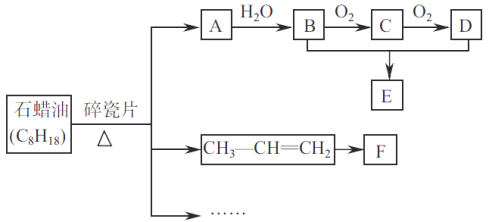
回答下列问题:
(1)A中所含官能团名称为_________________。由B和D生成E的化学方程式为________________。
(2)F为高分子化合物。可以用来制造汽车保险杠,其结构简式为__________________。
(3)设计实验证明A与溴水发生加成反应而不是取代反应__________________________。
(4)有机物X是石蜡油(C8H18)的同系物,分子中碳与氢的质量比为5:1,X的同分异构体共有____种,其中一氯代物只有一种的是__________(写结构简式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com