
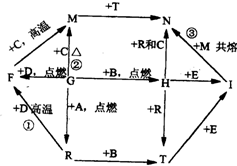
 ��ͼ��ʾ��A��B��C��D��G�����ֳ������ʣ�����A��GΪ���壮������R�ڳ����³�Һ̬��FΪ��ɫ���壬HΪ����ɫ��ĩ��I�Dz�����ҵ��һ��ԭ�ϣ�ͼ�в�������������ȥ���Իش��������⣺
��ͼ��ʾ��A��B��C��D��G�����ֳ������ʣ�����A��GΪ���壮������R�ڳ����³�Һ̬��FΪ��ɫ���壬HΪ����ɫ��ĩ��I�Dz�����ҵ��һ��ԭ�ϣ�ͼ�в�������������ȥ���Իش��������⣺ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
�� Fe3O4+4H2���ʴ�Ϊ��3Fe+4H2O
Fe3O4+4H2���ʴ�Ϊ��3Fe+4H2O Fe3O4+4H2��
Fe3O4+4H2�� 2NaAlO2+CO2�����ʴ�Ϊ��Na2CO3+Al2O3
2NaAlO2+CO2�����ʴ�Ϊ��Na2CO3+Al2O3 2NaAlO2+CO2����
2NaAlO2+CO2���� 2Al2O3����n��Al��=
2Al2O3����n��Al��=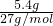 =0.2molʱ���ų�166.9kJ��������4molAl��Ӧ�ų�3338kJ����������Ӧ�ڵ��Ȼ�ѧ����ʽΪ4Al��S��+3O2��g��=2Al2O3��S����H=-3338kJ/mol��
=0.2molʱ���ų�166.9kJ��������4molAl��Ӧ�ų�3338kJ����������Ӧ�ڵ��Ȼ�ѧ����ʽΪ4Al��S��+3O2��g��=2Al2O3��S����H=-3338kJ/mol��

 ���Ž�������С״Ԫϵ�д�
���Ž�������С״Ԫϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��ͼ��ʾ��a��b��c��d��Ϊʯī�缫��ͨ��һ��ʱ����缫�ϵ�����������ʵ���֮������Ϊ4��1��2��2����ס��������еĵ���ʷֱ��ǣ�������
��ͼ��ʾ��a��b��c��d��Ϊʯī�缫��ͨ��һ��ʱ����缫�ϵ�����������ʵ���֮������Ϊ4��1��2��2����ס��������еĵ���ʷֱ��ǣ��������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
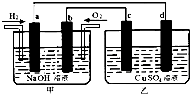 ��ͼ��ʾ��a��b��c��dΪ���Ե缫����װ����a��b�����缫�Ϸֱ�ͨ��H2��O2���������ҺΪNaOH��Һ����װ���е������ҺΪCuSO4��Һ�������й�˵����ȷ���ǣ�������
��ͼ��ʾ��a��b��c��dΪ���Ե缫����װ����a��b�����缫�Ϸֱ�ͨ��H2��O2���������ҺΪNaOH��Һ����װ���е������ҺΪCuSO4��Һ�������й�˵����ȷ���ǣ��������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��10L�ܱ������У�ij���ȷ�Ӧ���й����ڲ�ͬ��Ӧʱ������ʵ����ı仯�����ͼ��ʾ��A��B��C��Ϊ���壩����
��10L�ܱ������У�ij���ȷ�Ӧ���й����ڲ�ͬ��Ӧʱ������ʵ����ı仯�����ͼ��ʾ��A��B��C��Ϊ���壩�����鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com