
”¾ĢāÄæ”æ”¾Ń”ŠŽ3£ŗĪļÖŹµÄ½į¹¹ÓėŠŌÖŹ”æ¢ń.·śŌŖĖŲŹĒµēøŗŠŌ×ī“óµÄ·Ē½šŹōŌŖĖŲ£¬ĒŅ·śŌ×ӵİė¾¶Š”£¬Ņņ“Ė·śµ„ÖŹ¼«Ņ×ŗĶ½šŹōµ„ÖŹ·“Ó¦ĒŅ°ŃĖüĆĒŃõ»Æµ½×īøß¼ŪĢ¬£¬ČēMnF7 ”¢VF5 ”¢CaF2 µČ”£·śŌŖĖŲ»¹æÉŅŌŗĶŃõŌŖĖŲŠĪ³É·ś»ÆĪļ£¬ČēOF2 µČ”£
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ

£Ø1£©VŌ×ÓµÄŗĖĶāµē×ÓÅŲ¼Ź½ĪŖ ”£ČēĶ¼±ķŹ¾Ņ»øö²»ĶźÕūµÄCaF2 ¾§°ū£¬ŌņĶ¼ÖŠŹµŠÄĒņ±ķŹ¾ (Ģī”°F-»ņCa2+ )”£ Éč¾§°ū±ß³¤ĪŖa£¬Ōņ×ī½üµÄF-ŗĶCa2+Ö®¼äµÄ¾ąĄėĪŖ (ÓĆŗ¬aµÄ“śŹżŹ½±ķŹ¾)”£
£Ø2£©OF2 ·Ö×ÓÖŠŃõŌ×ӵĹģµĄŌÓ»ÆĄąŠĶĪŖ £¬OF2±»³ĘĪŖ·ś»ÆĪļ¶ų²»±»³ĘĪŖŃõ»ÆĪļµÄŌŅņŹĒ ”£
¢ņ.“æĶŌŚ¹¤ŅµÉĻÖ÷ŅŖÓĆĄ“ÖĘŌģµ¼Ļß”¢µēĘ÷ŌŖ¼žµČ£¬ĶÄÜŠĪ³É+1ŗĶ+2µÄ»ÆŗĻĪļ”£»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø3£©Š“³ö»łĢ¬Cu+ µÄŗĖĶāµē×ÓÅŲ¼Ź½ ”£C”¢N”¢OČżÖÖŌŖĖŲµÄµŚŅ»µēĄėÄÜÓɓ󵽊”µÄĖ³ŠņŹĒ ”£
£Ø4£©ČēĶ¼ĖłŹ¾ŹĒĶµÄijÖÖŃõ»ÆĪļµÄ¾§°ūŹ¾ŅāĶ¼£¬øĆŃõ»ÆĪļµÄ»ÆѧŹ½ĪŖ ”£
£Ø5£©ĻņĮņĖįĶČÜŅŗÖŠµĪ¼Ó°±Ė®»įÉś³ÉĄ¶É«³Įµķ£¬ŌŚµĪ¼Ó°±Ė®ÖĮ³ĮµķøÕČ«²æČܽāŹ±æɵƵ½Ą¶É«ČÜŅŗ£¬¼ĢŠųĻņĘäÖŠ¼ÓČė¼«ŠŌ½ĻŠ”µÄŅŅ“¼æÉŅŌÉś³ÉÉīĄ¶É«µÄ[Cu(NH3)4]SO4”¤H2O³Įµķ”£øĆÉīĄ¶É«³ĮµķÖŠµÄNH3Ķعż¼üÓėÖŠŠÄĄė×ÓCu2+½įŗĻ”£NH3·Ö×ÓÖŠµÄNŌ×ÓŌӻƷ½Ź½ŹĒ ”£ÓėNH3·Ö×Ó»„ĪŖµČµē×ÓĢåµÄŅ»ÖÖĪ¢Į£ŹĒ (ČĪŠ“Ņ»ÖÖ)
”¾“š°ø”æ£Ø1£©1s22s22p63s23p63d34s2 »ņ[Ar]3d34s2 (2·Ö)Ca2+ (1·Ö)![]() (3 ·Ö )
(3 ·Ö )
£Ø2£©sp3ŌÓ»Æ(1·Ö) Ńõ»ÆĪļÖŠŃõŌŖĖŲĻŌøŗ¼Ū£¬¶ųŌŚOF2ÖŠŃõŌŖĖŲµÄ»Æ½é¼ŪĪŖ+2 (1·Ö)
II£®£Ø3£©ls22s22p63s23p63d10»ņ”¾Ar”æ3d10(2·Ö) N”¢O”¢C (1·Ö)
£Ø4£©CuO (1·Ö) £Ø5£©ÅäĪ»(1·Ö) sp3ŌÓ»Æ (1·Ö) H3O+µČ(1·Ö)
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗ£Ø1£©VŌ×ÓŹĒ23ŗÅ£¬ĘäŗĖĶāµē×ÓÅŲ¼Ź½ĪŖ1s22s22p63s23p63d34s2(»ņ[Ar]3d34s2)£»CaF2¾§°ūÖŠ£¬°×ĒņµÄŹżÄæĪŖ8”Į1/8+6”Į1/2=4£¬ŗŚĒņČ«²æŌŚ¾§°ūÄŚ²æ£¬ŹżÄæĪŖ8£¬ŌņĶ¼ÖŠ°×ĒņŹĒøĘĄė×Ó£»°Ń¾§°ū·Ö³É8øöŠ”µÄĮ¢·½ĢåČēĶ¼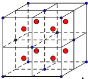 £¬ŌņF-Ī»ÓŚŠ”Į¢·½ĢåµÄÖŠŠÄ£¬¼“Š”ŗģĒņ£¬ŌņCa2+ÓėF-Ö®¼äµÄ×ī½ü¾ąĄėĪŖŠ”Į¢·½ĢåµÄĢå¶Ō½ĒĻßµÄŅ»°ė£¬ŅŃÖŖ¾§°ū±ß³¤ĪŖa£¬ŌņŠ”Į¢·½ĢåµÄ±ß³¤ĪŖa/2£¬ÉčCa2+ÓėF-Ö®¼äµÄ×ī½ü¾ąĄėĪŖx£¬
£¬ŌņF-Ī»ÓŚŠ”Į¢·½ĢåµÄÖŠŠÄ£¬¼“Š”ŗģĒņ£¬ŌņCa2+ÓėF-Ö®¼äµÄ×ī½ü¾ąĄėĪŖŠ”Į¢·½ĢåµÄĢå¶Ō½ĒĻßµÄŅ»°ė£¬ŅŃÖŖ¾§°ū±ß³¤ĪŖa£¬ŌņŠ”Į¢·½ĢåµÄ±ß³¤ĪŖa/2£¬ÉčCa2+ÓėF-Ö®¼äµÄ×ī½ü¾ąĄėĪŖx£¬
Ōņ(a/2)2+(a/2)2+(a/2)2=x2£¬½āµĆx=![]() £»
£»
£Ø2£©OF2·Ö×ÓÖŠŃõŌ×ÓĪŖ2+(6-2”Į1)/2=4£¬ŹōÓŚsp3Ōӻƣ»OF2ÖŠFŌŖĖŲĪŖ-1¼Ū£¬OŌŖĖŲµÄ»ÆŗĻ¼ŪĪŖ+2¼Ū£¬¶ųŃõ»ÆĪļÖŠOŌŖĖŲµÄ»ÆŗĻ¼ŪĪŖ-2¼Ū£¬ĖłŅŌOF2±»³ĘĪŖ·ś»ÆĪļ£»
£Ø3£©CuµÄŌ×ÓŠņŹżĪŖ29£¬¼Ūµē×ÓÅŲ¼ĪŖ3d104s1£¬Ōņ»łĢ¬Cu+µÄŗĖĶāµē×ÓÅŲ¼Ź½ĪŖ ls22s22p63s23p63d10»ņ”¾Ar”æ3d10£¬C”¢O”¢NŌŖĖŲ¶¼ŹĒµŚ¶žÖÜĘŚ·Ē½šŹōŌŖĖŲ£¬Ķ¬Ņ»ÖÜĘŚŌŖĖŲ×Ō×ó¶ųÓŅµŚŅ»µēĄėÄܳŹŌö“óĒ÷ŹĘ£¬µ«NŌŖĖŲŌ×Ó2pÄܼ¶ŹĒ°ėĀśĪȶØדĢ¬£¬ÄÜĮæ½ĻµĶ£¬µŚŅ»µēĄėÄÜøßÓŚĶ¬ÖÜĘŚĻąĮŚŌŖĖŲ£¬¹ŹµŚŅ»µēĄėÄÜN£¾O£¾C£»
£Ø4£©Óɾ§°ūŹ¾ŅāĶ¼æÉÖŖ£¬1øö¾§°ūÖŠÓŠ4øöA£¬BĪŖ8”Į1/8+6”Į1/2=4øö£¬Ō×ÓøöŹżÖ®±ČĪŖ1£ŗ1£¬øĆŃõ»ÆĪļµÄ»ÆѧŹ½ĪŖCuO£»
£Ø5£©NH3ÖŠNŌ×ÓĢį¹©¹Ā¶Ōµē×Ó£¬Cu2+Ģį¹©æÕ¹ģµĄ£¬¶žÕߊĪ³ÉÅäĪ»¼ü£»NH3·Ö×ÓÖŠ¹Ā¶Ōµē×ÓŹżĪŖ1£¬³É¼üŹżĪŖ3£¬ŌņNŌ×ÓµÄŌӻƷ½Ź½ĪŖsp3£¬ÓėNH3·Ö×Ó»„ĪŖµČµē×ÓĢåµÄŅ»ÖÖĪ¢Į£¾ßÓŠĻąĶ¬µÄ¼Ūµē×ÓŹż8ŗĶŌ×ÓŹż4£¬Ī¢Į£ĪŖPH3»ņH3O+µČ”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆĻąĶ¬Ģå»żµÄ0.1mol”¤ L-1µÄBaCl2ČÜŅŗ£¬ÄÜ·Ö±šŹ¹ĻąĶ¬Ģå»żµÄFe2(SO4)3”¢ZnSO4”¢Na2SO4ČÜŅŗµÄSO42-ĶźČ«³Įµķ£¬ŌņČżÖÖČÜŅŗµÄĪļÖŹµÄĮæÅضČÖ®±ČĪŖ£Ø £©
A. 3”Ć2”Ć1 B. 1”Ć2”Ć3 C. 3”Ć1”Ć1 D. 1”Ć3”Ć3
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ”°æɳ֊ųŌŁÉśµÄĀĢÉ«ÄÜŌ“”±ŹĒæĘѧ¼ŅÄæĒ°ÕżŌŚŃŠ¾æµÄŠĀÄÜŌ“Ö®Ņ»”£ĄūÓĆøßĮ»”¢ÓńĆ×µČĀĢÉ«Ö²ĪļµÄÖÖ×Ó[Ö÷ŅŖ³É·ÖŹĒµķ·Ū£ØC6H10O5£©n]£¬¾·¢½Ķ”¢ÕōĮó¾ĶæÉŅŌµĆµ½øĆÄÜŌ“ĪļÖŹ£¬ĖüŹĒ( )
A£®ĒāĘų B£®¾Ę¾« C£®¼×Ķé D£®æÉČ¼±ł
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ½«ÉŁĮ潚ŹōÄĘ·Ö±šĶ¶ČėĻĀĮŠĪļÖŹµÄĖ®ČÜŅŗÖŠ£¬·“Ó¦ŗóČÜŅŗÖŹĮæ¼õĒįµÄŹĒ(””””)
A. HCl B. K2SO4 C. NaOH D. CuSO4
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æA”«E¶¼ŹĒÓŠ»ś»ÆŗĻĪļ£¬AĪŖŅ»Č”“ś·¼ĻćĢž£¬BÖŠŗ¬ÓŠŅ»øö¼×»ł”£ĖüĆĒµÄ×Ŗ»Æ¹ŲĻµČēĻĀ£ŗ

Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
(1) A µÄĆū³ĘĪŖ_____________£»
(2)ÓÉBÉś³ÉCµÄ»Æѧ·½³ĢŹ½ĪŖ_______________________________£»
(3)ÓÉBÉś³ÉD”¢ÓÉCÉś³ÉDµÄ·“Ó¦Ģõ¼ž·Ö±šŹĒ________”¢ ________ ”£
(4)ÓÉAÉś³ÉB”¢ÓÉDÉś³ÉEµÄ·“Ó¦ĄąŠĶ·Ö±šŹĒ________”¢ ________ ”£
(5)ŌŚEµÄĶ¬·ÖŅģ¹¹ĢåÖŠ£¬±½»·ÉĻŅ»Ļõ»ÆµÄ²śĪļÖ»ÓŠŅ»ÖֵĹ²ÓŠ___ÖÖ£¬ĘäÖŠŗĖ“Ź²ÕńĒāĘ×ÓŠĮ½×é·å£¬ĒŅ·åĆ껿±ČĪŖ1”Ć1µÄŹĒ_____(Ģī½į¹¹¼ņŹ½) ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ×Č¼”¢Ņ×±¬µČĪ£ĻÕ»ÆѧʷµÄ°ü×°Ó¦±źÓŠĻąÓ¦¾Æøę±źÖ¾”£ÅØĮņĖį°ü×°ÉĻµÄ±źÖ¾ĪŖ
A. øÆŹ“Ę·B. Ņ×Č¼Ę·C. ¾ē¶¾Ę·D. ±¬ÕØĘ·
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄæĒ°ŹĄ½ēÉĻ60%µÄĆ¾ŹĒ“Óŗ£Ė®ÖŠĢįČ”µÄ£®Ö÷ŅŖ²½ÖčČēĻĀ£ŗ
ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø £©
A. ĪŖŹ¹ŗ£Ė®ÖŠµÄMgSO4×Ŗ»Æ³ÉMg£ØOH£©2£¬ŹŌ¼Į¢ŁæÉŃ”ŌńŹÆ»ŅČé
B. ¼ÓČėŹŌ¼Į¢Łŗó£¬·ÖĄėµĆµ½Mg£ØOH£©2³ĮµķµÄ·½·ØŹĒ¹żĀĖ
C. ¼ÓČėŹŌ¼Į¢Ś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗOH©+H+=H2O
D. Ķعżµē½āČŪČŚµÄĪŽĖ®MgCl2µĆµ½48gMg£¬¹²×ŖŅĘ4molµē×Ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A. Ē¦Šīµē³Ų³äµēŹ±£¬Ńō¼«ÖŹĮæŌö“ó
B. 0.1mol ”¤L-lCH3COONaČÜŅŗ¼ÓČČŗó£¬ČÜŅŗµÄpH¼õŠ”
C. ±ź×¼×“æöĻĀ£¬11.2L±½ÖŠŗ¬ÓŠµÄĢ¼Ō×ÓŹżĪŖ3”Į6.02”Į1023
D. ŹŅĪĀĻĀ£¬Ļ”ŹĶ0.1mol”¤L-1°±Ė®£¬c(H+)”¤c(NH3”¤H2O)µÄÖµ¼õŠ”
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄæĒ°ŹĄ½ēÉĻ60%µÄĆ¾ŹĒ“Óŗ£Ė®ÖŠĢįČ”µÄ”£ŗ£Ė®ĢįĆ¾µÄÖ÷ŅŖĮ÷³ĢČēĻĀ£ŗ

ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A. ŌŚŗ£Ė®ÖŠ¼ÓČėŹÆ»ŅČéµÄ×÷ÓĆŹĒ³ĮµķMg2£«
B. æÉÓƵē½āĀČ»ÆĆ¾µÄ·½·Ø»ńµĆĆ¾
C. ²Ł×÷BÉę¼°µ½¼ÓČČÅØĖõ(»ņÕō·¢½į¾§)”¢¹żĀĖµČ²Ł×÷
D. ÉĻŹö¹ż³ĢÖŠÖ»Éę¼°µ½Ńõ»Æ»¹Ō·“Ó¦ŗĶø“·Ö½ā·“Ó¦
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com