
【题目】将2.7 g铝和4.6 g钠同时加入足量的水中充分反应,将反应后的溶液稀释、定容为500 mL。下列说法中正确的是
A. 所得溶液中阳离子和阴离子的物质的量之比为1∶1
B. 参加反应的水的质量与加入铝的质量相等
C. 所得溶液中钠离子和铝离子物质的量之比为2∶1
D. 反应中放出的气体在标准状况下的体积为2.24 L
【答案】A
【解析】
先根据钠与水反应方程式求出氢氧化钠的物质的量,再根据Al与氢氧化钠反应计算判断。
4.6g钠的物质的量为 ![]() =0.2mol,2.7gAl的物质的量为
=0.2mol,2.7gAl的物质的量为![]() =0.1mol。根据Na和水的反应:2 Na+2H2O═2 NaOH+H2↑知,生成的n(NaOH)=0.2mol,根据NaOH和Al的反应:2 Al+2 NaOH+2H2O═2 NaAlO2 +3 H2↑知,NaOH过量,Al完全反应,反应后溶液中的溶质为0.1molNaAlO2、0.1molNaOH。A、因反应后溶液中含有0.1molNaAlO2、0.1molNaOH,阳离子和阴离子的物质的量之比为1∶1,故A正确;B、根据NaOH和Al的反应:2 Al+2 NaOH+2H2O═2 NaAlO2 +3 H2↑知,反应共消耗水0.3mol,质量为5.4g,Al的物质的量为0.1mol,质量为2.7g,质量不等,故B错误;C、因反应后溶液中含有0.1molNaAlO2、0.1molNaOH,没有Al3+,故C错误;D、因钠与水反应和铝与氢氧化钠反应都放出气体,气体在标准状况下的体积为22.4L/mol×(
=0.1mol。根据Na和水的反应:2 Na+2H2O═2 NaOH+H2↑知,生成的n(NaOH)=0.2mol,根据NaOH和Al的反应:2 Al+2 NaOH+2H2O═2 NaAlO2 +3 H2↑知,NaOH过量,Al完全反应,反应后溶液中的溶质为0.1molNaAlO2、0.1molNaOH。A、因反应后溶液中含有0.1molNaAlO2、0.1molNaOH,阳离子和阴离子的物质的量之比为1∶1,故A正确;B、根据NaOH和Al的反应:2 Al+2 NaOH+2H2O═2 NaAlO2 +3 H2↑知,反应共消耗水0.3mol,质量为5.4g,Al的物质的量为0.1mol,质量为2.7g,质量不等,故B错误;C、因反应后溶液中含有0.1molNaAlO2、0.1molNaOH,没有Al3+,故C错误;D、因钠与水反应和铝与氢氧化钠反应都放出气体,气体在标准状况下的体积为22.4L/mol×(![]() +
+![]() ×0.1mol)=5.6L,故D错误;故选A。
×0.1mol)=5.6L,故D错误;故选A。


科目:高中化学 来源: 题型:
【题目】下图为一定条件下采用多孔惰性电极的储氢电池充电装置(忽略其他有机物)。
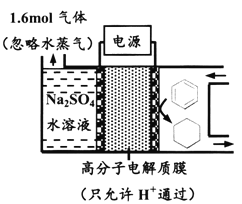
已知储氢装置的电流效率![]() 100%,下列说法不正确的是
100%,下列说法不正确的是
A. 若η=75%,则参加反应的苯为0.8mol
B. 过程中通过C—H键断裂实现氢的储存
C. 采用多孔电极增大了接触面积,可降低电池能量损失
D. 生成目标产物的电极反应式为:C6H6+6e-+6H+=C6H12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示装置,可用来制取和观察Fe(OH)2在空气中被氧化的颜色变化。实验时必须使用铁屑和6 mol·L-1的硫酸,其他试剂任选。

填写下列空白:
(1)B中盛有一定量的NaOH溶液,A中应预先加入的是________,A中反应的离子方程式是________。
(2)实验开始时应先将活塞a打开,其目的是____________________。
(3)简述生成Fe(OH)2的操作过程:_______________________
(4)实验完毕,打开b处活塞,放入一部分空气,此时B中发生反应的化学方程式为____。
(5)图中________(填“能”或“不能”)较长时间看到Fe(OH)2白色沉淀。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某恒温固定体积为2 L密闭容器中,发生反应:2SO2(g)+ O2(g) ![]() 2SO3(g) ΔH <0,n(SO2)随时间的变化如表:
2SO3(g) ΔH <0,n(SO2)随时间的变化如表:
时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
n(SO2)/mol | 0.20 | 0.16 | 0.13 | 0.11 | 0.08 | 0.08 |
则下列说法正确的是
A. 当容器中气体的密度不变时,说明该反应已达到平衡状态
B. 用O2表示0~4 min内该反应的平均速率为0.005 mol/(L·min)
C. 若升高温度,则SO2的反应速率会变大,平衡常数K值会增大
D. 平衡时再通入18O2,平衡右移,再次平衡时各物质均含有18O,O2的转化率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2A(g) ![]() 2B(g)+C(g)在恒定容积密闭容器中反应,下列选项中不能说明反应已达到平衡状态的是
2B(g)+C(g)在恒定容积密闭容器中反应,下列选项中不能说明反应已达到平衡状态的是
A. 混合气体中A与B的物质的量之比保持恒定
B. 容器内气体总压强不再改变的状态
C. 用A、B、C的物质的量浓度变化表示的反应速率的比为2:2:1
D. 混合气体的平均相对分子质量不再改变的状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把碎纸片b补充到a中,可得到一个完整的离子方程式(未配平),下列说法正确的是

A. 反应物微粒是S、SO32-、OH-
B. 3mol S参加反应时,转移的电子数3NA
C. 氧化剂与还原剂的物质的量之比为1:2
D. 该反应说明S2-和SO32-在碱性溶液中可以大量共存
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A. 同一原子中,2p、3d、4f能级的轨道数依次增多
B. 电子排布(23V)1s22s22p63s23p63d5违反了洪特规则
C. 原子核外电子的每一个能层最多可容纳的电子数为2n2
D. ![]() 违反了泡利不相容原理
违反了泡利不相容原理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
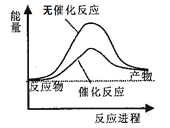
A. 如图可表示水分解过程中的能量变化
B. 若2C(s)+O2(g)=2CO(g)△=221.0kJ/mol,则碳的燃烧热为110.5kJ/mol
C. 需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应
D. 已知I:反应H2(g)+Cl2(g)=2HCl(g)△=akJ/mol,II:![]() 且a、b、c均大于零,则断开1mol HCl键所需的能量为(abc)kJ/mol
且a、b、c均大于零,则断开1mol HCl键所需的能量为(abc)kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com