
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| a(V2-V1) |
| V |
| a(V2-V1) |
| V |
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.下列有关实验操作中,合理的是_____(填序号)。
A.用托盘天平称取11.70 g食盐
B.用量筒量取12.36 mL盐酸
C.用酸式滴定管量取21.20 mL 0.10 mol/L H2SO4溶液
D.用200 mL容量瓶配制500mL 0.1 mol/L NaCl溶液
E.测定溶液的pH时,用洁净、干燥的玻璃棒蘸取溶液,滴在用蒸馏水润湿过的pH试纸上,再与标准比色卡比较
Ⅱ.现用物质的量浓度为a mol/L的标准盐酸装在滴定管中去测定V mL NaOH溶液的物质的量浓度,请填写下列空白:
(1)酸式滴定管用蒸馏水洗净后,还应该进行的操作是______ ____。
(2)若在滴定前滴定管尖嘴部分留有气泡,滴定后滴定管尖嘴部分气泡消失,则测定的NaOH物质的量浓度__(选填“偏大”、“偏小”或“无影响”)
Ⅲ、在由锌和石墨作两极材料、硫酸钠与硫酸铜组成的混合溶液作电解质溶液所形成的原电池中,正极上发生的反应的电极反应式是: 。
查看答案和解析>>
科目:高中化学 来源:2010年广西桂林十八中高二上学期期中考试化学卷 题型:填空题
Ⅰ.下列有关实验操作中,合理的是_____(填序号)。
| A.用托盘天平称取11.70 g食盐 |
| B.用量筒量取12.36 mL盐酸 |
| C.用酸式滴定管量取21.20 mL 0.10 mol/L H2SO4溶液 |
| D.用200 mL容量瓶配制500 mL 0.1 mol/L NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源:2013届内蒙古巴彦淖尔市高二期中考试化学试卷 题型:实验题
(16分)Ⅰ.下列有关实验操作中,合理的是______________(填序号) 。
A.用托盘天平称取11.70g食盐 B.用量筒量取12.36mL盐酸
C.用酸式滴定管量取21.20mL0.10mol/L H2SO4溶液
D.用200mL容量瓶配制500mL0.1mol/L NaCl溶液
E.测定溶液的pH时,用洁净、干燥的玻璃棒蘸取溶液,滴在用蒸馏水润湿过的pH试纸上,再与标准比色卡比较
Ⅱ.现用物质的量浓度为a mol/L的标准盐酸去测定V mL NaOH溶液的物质的量浓度,请填写下列空白:(1)酸式滴定管用蒸馏水洗净后,还应该进行的操作是_______________________。
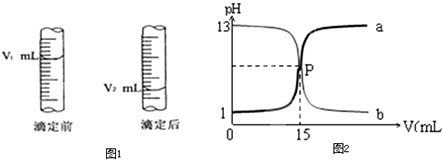
(2)下图是酸式滴定管中液面在滴定前后的读数:c (NaOH) = _____mol/L。

(3)若在滴定前滴定管尖嘴部分留有气泡,滴定后滴定管尖嘴部分气泡消失,则测定的NaOH物质的量浓度______。(选“偏大”“偏小”“不变”)
III.如图是盐酸与氢氧化钠的滴定曲线a和b,试认真分析后填空:

曲线a是用 溶液滴定 溶液;曲线b是用 溶液滴定 溶液;P点的坐标为( );盐酸的物质的量浓度为 mol/L。
查看答案和解析>>
科目:高中化学 来源:2010年黑龙江牡丹江一中高二上学期期中考试化学试卷 题型:实验题
Ⅰ.下列有关实验操作或结果的说法中正确的是 (填字母)
A.滴定时,眼睛应始终注视滴定管内液面的变化
B.用碱式滴定管量取0.10 mol·L-1的KMnO4溶液15.10 mL
C.酸碱中和滴定之前,锥形瓶用蒸馏水洗净即可,不能用待测液润洗
D.用pH试纸测量某溶液的pH时要先将试纸润湿
E.滴定管经蒸馏水洗净后,直接注入标准液,将使测得的待测液浓度偏高
F.用广泛pH试纸测量H2SO4溶液的pH时,测得pH=3.2
G.测定酸碱滴定曲线:开始时测试和记录的间隔可稍小些,滴定至终点附近则要大些
Ⅱ.(1)由氢气和氧气反应生成1 mol水蒸气放热241.8kJ,写出该反应的热化学方程式 。已知H2O(l) = H2O(g) ΔH =+44 kJ·mol-1 则标准状况下33.6 L H2 生成液态水时放出的热量是 kJ。
(2)化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量。已知白磷P4和P4O6的分子结构如下图所示:
现提供以下化学键的键能:P-P 198 kJ·mol-1 P-O 360 kJ·mol-1,氧气分子内氧原子间的(O=O)键能为498 kJ·mol-1。则P4+3O2 = P4O6的反应热ΔH为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com