
分析 (1)H2S是二元弱酸,属弱电解质,分两步电离,第一步电离出氢离子和硫氢根离子,第二步电离为硫氢根离子电离出硫离子和氢离子,以第一步电离为主;
(2)当向H2S溶液中加入NaOH固体时,OH-与H+反应,硫化氢的电离平衡正移,c(S2-)增大,c(H+)减小;
(3)若向原饱和溶液中加入无水硫酸铜粉末,生成CuS沉淀,平衡向右移动,据此分析解答.
解答 解:(1)H2S是二元弱酸,属弱电解质,分两步电离,第一步电离出氢离子和硫氢根离子,第二步电离为硫氢根离子电离出硫离子和氢离子,电离方程式为:H2S?H++HS-,HS-?H++S2-;以第一步电离为主,所以c(HS-)>c(S2-),两步电离均有氢离子生成,所以c (HS-)<c(H+),c(H+)>c(S2-);
故答案为:H2S?H++HS-,HS-?H++S2-;>;<;>;
(2)H2S溶液中存在着H2S=H++HS-、HS-=H++S2-的平衡,当向H2S溶液中加入NaOH固体时,OH-与H+反应,减少生成物的浓度,平衡向正方向移动,所以c(H+)减小,c(S2-)增大,
故答案为:增大;增大;减小;
(3)H2S溶液中存在着H2S=H++HS-、HS-=H++S2-的平衡,若向原饱和溶液中加入无水硫酸铜粉末,生成CuS沉淀,c(S2-)减小,平衡向正方向移动,c(H+)增大;
故答案为:减小;正方向;增大.
点评 本题考查了弱电解质的电离,明确影响弱电解质电离的因素是解本题关键,题目难度不大,注意多元弱酸分步电离以第一步电离为主.


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 共价键 | H-H | F-F | H-F | H-Cl | H-I |
| E(kJ•mol-1 ) | 436 | 157 | 568 | 432 | 298 |
| A. | 432 kJ•mol -1>E(H-Br)>298 kJ•mol -1 | |
| B. | 表中最稳定的共价键是H-F键 | |
| C. | H 2 (g)→2H (g)△H=+436 kJ•mol -1 | |
| D. | H 2 (g)+F 2 (g)=2HF(g)△H=-25 kJ•mol -1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 需要加热发生的反应一定是吸热反应 | |
| B. | 任何放热反应在常温下一定能发生 | |
| C. | 温度压强一定时,放热的、熵增加反应能自发进行 | |
| D. | 吸热反应一定是反应物总能量大于生成物的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | c(HCOO-)<c(Na+) | B. | c(HCOO-)>c(Na+) | C. | c(OH-)>c(HCOO-) | D. | c(OH-)<c(HCOO-) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Ca2CO3+2HCl═CaCl2+H2O+CO2↑ | B. | 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$ 2H2O+O2↑ | ||
| C. | Cu+4HNO3(稀)═Cu(NO3)2+2NO↑+2H2O | D. | NaCl+AgNO3═AgCl↓+NaNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
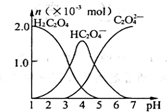 常温下,向10mL 0.2mol•L-1草酸(H2C2O4)溶液中逐滴加入等浓度的NaOH溶液.有关微粒的物质的量与混合溶液的pH有如图关系,下列说法正确的是
常温下,向10mL 0.2mol•L-1草酸(H2C2O4)溶液中逐滴加入等浓度的NaOH溶液.有关微粒的物质的量与混合溶液的pH有如图关系,下列说法正确的是| A. | HC2O4-在溶液中水解程度大于电离程度 | |
| B. | 当V(NaOH)=10 mL,时,溶液中水的电离程度比纯水大 | |
| C. | 当V(NaOH)=15 mL,时,溶液中存在:c(Na+)>c(HC2O4-)>c(C2O42-)>c(OH-)>c(H+) | |
| D. | 当V(NaOH)=20 mL,时,溶液中存在:c(OH-)=c(HC2O4-)+2c(H2C2O4)+c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com